Polivinil spirti
Naviqasiyaya keçin
Axtarışa keçin
| Polivinil spirti | |
|---|---|
 | |
 | |
| Fiziki xassələri | |
| Sıxlıq | 1,269 q/sm³[1] |
| Təsnifatı | |
| CAS-da qeyd. nöm. | 9002-89-5 |
| RTECS | TR8100000 |
| ChEBI | 17246 |
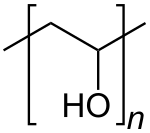
Poli (vinil spirti) (PVOH, PVA, və ya PVAl) — suda həll olunan sintetik polimer. İdeallaşdırılmış [CH2CH(OH)]n formulaya malikdir. Kağız istehsalında, toxuculuq çubuqlarının ölçüsünün təyin olunmasında, polivinil asetat (PVAc) yapışdırıcı formulalarında qatılaşdırıcı və emulsiya stabilizatoru kimi, müxtəlif örtüklərdə və 3D çapda istifadə olunur. Rəngsiz (ağ) və qoxusuzdur. Adətən muncuqlar və ya suda məhlullar şəklində təqdim olunur.[2][3] Xaricdən əlavə edilmiş çarpaz bağlayıcı agent olmadan, PVA məhlulu təkrar dondurma-ərimə yolu ilə jelə çevrilə bilər, damar stentləri, qığırdaq, kontakt linzalar və s. kimi müxtəlif tətbiqlərdə istifadə olunan yüksək güclü, ultra təmiz, biouyğun hidrojellər istehsal edir.[4]
İstinadlar[redaktə | mənbəni redaktə et]
- ↑ https://www.sigmaaldrich.com/MSDS/MSDS/DisplayMSDSPage.do?country=CZ&language=cs&productNumber=341584&brand=ALDRICH&PageToGoToURL=https%3A%2F%2Fwww.sigmaaldrich.com%2Fcatalog%2Fsearch%3Fterm%3D9002-89-5%26interface%3DCAS%2520No.%26N%3D0%26mode%3Dpartialmax%26lang%3Den%26region%3DCZ%26focus%3Dproduct.
- ↑ Şablon:Ullmann
- ↑ Tang X, Alavi S. "Recent Advances in Starch, Polyvinyl Alcohol Based Polymer Blends, Nanocomposites and Their Biodegradability". Carbohydrate Polymers. 85. 2011: 7–16. doi:10.1016/j.carbpol.2011.01.030.
- ↑ Adelnia, Hossein; Ensandoost, Reza; Shebbrin Moonshi, Shehzahdi; və b. "Freeze/thawed polyvinyl alcohol hydrogels: Present, past and future". European Polymer Journal (ingilis). 164. 2022-02-05: 110974. doi:10.1016/j.eurpolymj.2021.110974. ISSN 0014-3057. 2023-01-04 tarixində arxivləşdirilib. İstifadə tarixi: 2023-06-02.