Telofaza

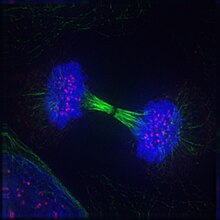
Telofaza — Telofaza (yunanca τέλος (télos), "son" və φάσις (phásis), "mərhələ") - eukariotik bir hüceyrədə həm meyozda, həm də mitozda son mərhələdir. Telofaza zamanı profaza və prometafazanın (nukleolus və nüvə membranının parçalanması) təsiri əksinə olur. Xromosomlar hüceyrə qütblərinə çatdıqda, hər bir xromatid ətrafında nüvə zərfləri yenidən yığılır, nukleollar yenidən ortaya çıxır və xromosomlar yenidən faza zamanı mövcud olan genişlənmiş xromatinə dekondensasiya olunmağa başlayır. Mitotik saplar sökülür və mikroxovlar depolimerləşdirilir. Telofaza hüceyrə dövrü müddətinin təxminən 2%-ni təşkil edir. Sitokinez, adətən, telofazadan əvvəl başlayır və tamamlandıqda, bir cüt ayrı qız hüceyrə arasında iki qız nüvəsini ayırır[1].
Substratların fosforlaşması[redaktə | mənbəni redaktə et]
Hədəf zülalların fosforlaşması erkən mitozda sapların yığılmasını, xromosom kondensasiyasını və nüvə pərdələrinin məhv edilməsini idarə edir. Eyni substratların fosforlaşması sapların sökülməsinə, xromosomların dekondensasiyasına və telofazada qız nüvələrinin yenidən formalaşmasına səbəb olur[2]. Telofaza hadisələrini həll edən defosforlaşma dərəcəsinin qurulması həm inaktivləşdirilməsini, həm də fosfatazaların aktivləşməsini tələb edir[3] .
Telofazanı tənzimləyən əlavə mexanizmlər[redaktə | mənbəni redaktə et]
Bütün hüceyrəli fosfoprotein profilindəki dəyişiklik, fərdi telofaza hadisələrinin meydana gəlməsinə kömək edən bir çox tənzimləyici mexanizmdən yalnız ən genişidir[4].
Nüvə qabığının yenidən yığılması[redaktə | mənbəni redaktə et]
Nüvə qabığının əsas komponentləri ikiqat membran, nüvə məsamələri kompleksləri və nüvə membranının içinə daxil olan nüvə pərdəsidir. Bu komponentlər, profil və prometafaza zamanı sökülür və nüvə zərfinin ayrılmış xromatidlərin səthində telofaza zamanı yenidən qurulur[5] . Nüvə membranı prometafaza zamanı endoplazmik şəbəkə tərəfindən parçalanır və qismən əmilir və daxili nüvə membranı zülalı olan xromatinə hədəflənməsi bu prosesin əks istiqamətindəki telofaza zamanı baş verir[5] .
Mitoz zamanı nüvə membranının endoplazmik şəbəkə tərəfindən udulduğu hüceyrələrdə, yenidən yığılma, xromatin səthində genişlənən membranın sabitləşməsi ilə xromatin ətrafında genişlənməni əhatə edir [6] . Bu mexanizmin nüvə məsamələrinin əmələ gəlməsi üçün bir şərt olduğunu irəli sürən tədqiqatlar, çılpaq xromatinlə əlaqəli komplekslərinin əvvəlcədən məsamələr deyil, ayrı-ayrı vahidlər şəklində olduğunu göstərdi[7] . Zərf hamarlanır və genişlənir, bütün xromatid dəstini əhatə edir. Bu, ehtimal ki, davamlı membran içərisində qala bilən nüvə məsamələrindən laminat idxalı ilə əlaqədardır[8]. Xenopus yumurta ekstraktlarının nüvə qabıqları, laminatın nüvə idxalı maneə törədildikdə, qırışları qalmış və qatılaşdırılmış xromosomlarla sıx əlaqəli olduqda düzləşə bilmədi. Lakin, endoplazmatik şəbəkənin genişlənməsi halında, nüvə idxalı nüvə qabığının yenidən yığılması tamamlanmadan başlamış olur ki, bu da inkişaf edən nüvənin distal və medial aspektləri arasında keçici nüvə nüvəli protein qradiyentinə gətirib çıxarır[9] .
Profazda parçalanmış lamin alt bölmələri mitoz zamanı inaktivləşdirilir və ayrılır[10]. Laminatın yenidən yığılması, laminanın defosforiləşməsi (və əlavə olaraq lamin-B üzərindəki COOH qalıqlarının metilterifikasiyası ilə) tərəfindən sitimullaşdırılır. Lamin-B, anafazanın ortasında olan xromatin üzərində hərəkət edə bilir[3][11]. Telofaza zamanı, nüvə idxalı yenidən qurulduqda, lamin-A islahatın nüvəsinə daxil olur, lakin G1 fazasında bir neçə saat ərzində yavaş-yavaş periferik laminaya yığılmağa davam edir[12][13].
Maya laminlərdən məhrumdur nüvə zərfləri mitoz zamanı toxunulmaz qalır və sitokinez zamanı nüvə parçalanması baş verir[14].
Xromosomların dekondensasiyası[redaktə | mənbəni redaktə et]
Xromosomun genişlənmiş xromatinə dekondensasiyası (eyni zamanda boşalma və ya dekondensasiya olaraq da bilinir) genişlənmiş xromatinə çevrilməsi hüceyrələrin interfaza proseslərini bərpa etməsi üçün lazımdır və bir çox eukariotlarda telofaza zamanı nüvə zərfinin yığılması ilə paralel olaraq baş verir[15] . Onurğalılarda xromosomların dekondensasiyası yalnız nüvə idxalının bərpasından sonra başlayır[16][17].
İstinadlar[redaktə | mənbəni redaktə et]
- ↑ Reece, Jane; Urry, Lisa; Cain, Michael; Wasserman, Steven; Minorsky, Peter; Jackson, Robert (2011). Campbell Biology (10th ed.). Pearson. ISBN 978-0-321-77565-8.
- ↑ Clarke PR, Zhang C. "Spatial and temporal control of nuclear envelope assembly by Ran GTPase". Symposia of the Society for Experimental Biology (56). 2004: 193–204. PMID 15565882.
- ↑ 1 2 Morgan, David. The Cell Cycle. London, UK: New Science Press Ltd. 2007. 154–155. ISBN 978-0-9539181-2-6.
- ↑ Juang YL, Huang J, Peters JM, McLaughlin ME, Tai CY, Pellman D. "APC-mediated proteolysis of Ase1 and the morphogenesis of the mitotic spindle". Science. 275 (5304). February 1997: 1311–4. doi:10.1126/science.275.5304.1311. PMID 9036857.
- ↑ 1 2 Alberts B, Johnson A, Lewis J, Morgan D, Raff M, Roberts K, Walter P. Molecular Biology of the Cell (6th). New York, NY: Garland Science, Taylor and Francis Group. 2015. 995–996. ISBN 978-0-8153-4432-2.
- ↑ Inzé, Dirk. Cell Cycle Control and Plant Development. Oxford, UK: Blackwell Publishing Ltd. 2007. 99–103. ISBN 978-1-4051-5043-9.
- ↑ Afonso O, Matos I, Maiato H. "Spatial control of the anaphase-telophase transition". Cell Cycle. 13 (19). 2014: 2985–6. doi:10.4161/15384101.2014.959853. PMC 4614036. PMID 25486554.
- ↑ Monje-Casas, Fernando; Queralt, Ethel. The Mitotic Exit Network. New York, NY: Humana Press. 2017. 3–8. ISBN 9781493965007.
- ↑ Yellman CM, Roeder GS. "Cdc14 Early Anaphase Release, FEAR, Is Limited to the Nucleus and Dispensable for Efficient Mitotic Exit". PLOS ONE. 10 (6). 2015: e0128604. Bibcode:2015PLoSO..1028604Y. doi:10.1371/journal.pone.0128604. PMC 4474866. PMID 26090959.
- ↑ Fukushima K, Wang M, Naito Y, Uchihashi T, Kato Y, Mukai S, Yabuta N, Nojima H. "GAK is phosphorylated by c-Src and translocated from the centrosome to chromatin at the end of telophase". Cell Cycle. 16 (5). March 2017: 415–427. doi:10.1080/15384101.2016.1241916. PMC 5351929. PMID 28135906.
- ↑ Cao K, Nakajima R, Meyer HH, Zheng Y. "The AAA-ATPase Cdc48/p97 regulates spindle disassembly at the end of mitosis". Cell. 115 (3). October 2003: 355–67. doi:10.1016/S0092-8674(03)00815-8. PMID 14636562.
- ↑ Hetzer M, Meyer HH, Walther TC, Bilbao-Cortes D, Warren G, Mattaj IW. "Distinct AAA-ATPase p97 complexes function in discrete steps of nuclear assembly". Nature Cell Biology. 3 (12). December 2001: 1086–91. doi:10.1038/ncb1201-1086. PMID 11781570.
- ↑ Gay S, Foiani M. "Nuclear envelope and chromatin, lock and key of genome integrity". International Review of Cell and Molecular Biology. 317. 2015-01-01: 267–330. doi:10.1016/bs.ircmb.2015.03.001. ISBN 9780128022801. PMID 26008788.
- ↑ Aist JR. "Mitosis and motor proteins in the filamentous ascomycete, Nectria haematococca, and some related fungi". International Review of Cytology. 212. 2002-01-01: 239–63. doi:10.1016/S0074-7696(01)12007-3. ISBN 9780123646163. PMID 11804038.
- ↑ Woodruff, Jeffrey Blake. Mechanisms of Mitotic Spindle Disassembly and Positioning in Saccharomyces cerevisiae (Tezis) (ingilis). UC Berkeley. 2011. 2022-05-30 tarixində arxivləşdirilib. İstifadə tarixi: 2021-10-04.
- ↑ Woodruff JB, Drubin DG, Barnes G. "Mitotic spindle disassembly occurs via distinct subprocesses driven by the anaphase-promoting complex, Aurora B kinase, and kinesin-8". The Journal of Cell Biology. 191 (4). November 2010: 795–808. doi:10.1083/jcb.201006028. PMC 2983061. PMID 21079246.
- ↑ Dimitrova DS, Prokhorova TA, Blow JJ, Todorov IT, Gilbert DM. "Mammalian nuclei become licensed for DNA replication during late telophase". Journal of Cell Science. 115 (Pt 1). January 2002: 51–9. doi:10.1242/jcs.115.1.51. PMC 1255924. PMID 11801723.