Dibenzotiofen
| Dibenzotiofen | |
|---|---|
 | |
 | |
| Ümumi | |
| Kimyəvi formulu | C₁₂H₈S[1] |
| Molyar kütlə | 184,26 q/mol |
| Termik xüsusiyyətlər | |
| Ərimə nöqtəsi | 99 °C[2] |
| Qaynama nöqtəsi | 332,5 ± 1 °C |
| Təsnifatı | |
| CAS-da qeyd. nöm. | 132-65-0 |
| PubChem | 24893734 |
| BS-də qeydiyyat nömrəsi | 205-072-9 |
| RTECS | HQ3490550 |
| ChEBI | 23681 |
| ChemSpider | 2915 |
Dibenzotiofen — kimyəvi formulu C12H8S olan üç qatılaşdırılmış tsikldan ibarət üzvi heterosiklik maddədir: bir tiofen və iki benzol tsikli.
Alınması
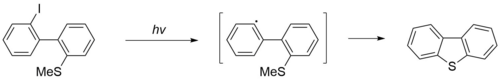
[redaktə | mənbəni redaktə et]Dibenzotiofen bir neçə yolla sintez edilə bilər. Birinci üsul ultrabənövşəyi radiasiyanın (civə lampası) təsiri altında 45–60 saat ərzində 2-yod-2'-metiltiobifenilin radikal tsiklləşməsindən ibarətdir.
Digər üsul tiol qrupunda allil bromidlə alkilləşən və karboksil qrupunda fenil efiri əmələ gələn tiosalisil turşusunun istifadəsinə əsaslanır. Alınmış birləşmənin 650 °C-də vakuumda pirolizindən 88% səmərə ilə dibenzotiofen əldə edilir.
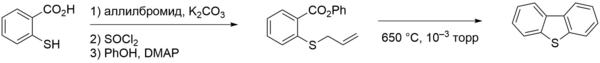
Molekuldaxili aromatik elektrofil əvəzetmə reaksiyasına əsaslanan dibenzotiofenin alınması üsulu da işlənib hazırlanmışdır. 2-Brombifenil, bromun litiumla əvəz edilməsinə məruz qalır və halogenin yerinə bir metiltiol qrupu əmələ gələrək, dimetil disulfid ilə reaksiyaya girir. Sonra sulfoksidə oksidləşir, bundan sonra trifluormetansülfonil turşusunun təsiri altında dehidratasiyaya uğrayır , elektrofil tsiklləşməyə daxil edilir. Yaranan məhsulun demetiləşməsi dibenzotiofenə gətirib çıxarır:
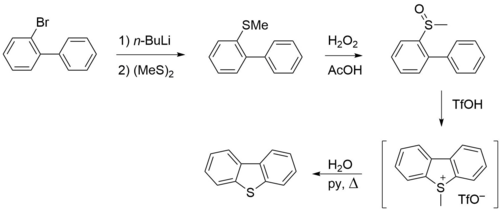
Dibenzotiofen benzinin aralıq məhsulunun anion tsiklləşməsi əsaslanan üsulla alınmışdır. Bunun üçün birinci mərhələdə 2-florotiofenol (Ulmana görə) mis oksidin iştirakı ilə 2-xlornitrobenzol ilə kombinasiyaya daxil edilir. Sonra nitro qrup dəmirlə reduksiya edilir və nəticədə yaranan amin qrup yodla əvəz olunur. Üçlübutil litium ilə təmizləmə dibenzofurana gətirib çıxarır:
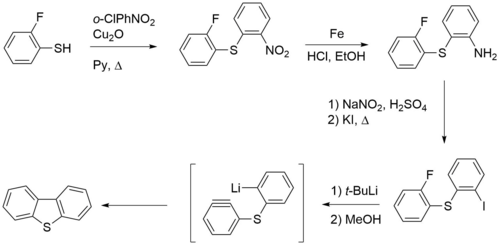
Beləliklə, dibenzotiofen 2,2'-diyodbifenildən və kükürd xammalı olan kalium sulfid və ya karbon disulfiddən sintez edilə bilər:
Kimyəvi xassələri
[redaktə | mənbəni redaktə et]Dibenzotiofen kükürd atomunun donor aktivliyinə görə 2 və 8-ci mövqelərdə halogenləşir. Əgər o, sulfona oksidləşirsə, onda qrup akseptor olur və halogenləşmə 3 və 7-ci mövqelərdə baş verir. Çox vaxt dibenzotiofen yodlaşdırılır, bromlaşdırılır və nəticədə halogen törəmələri daha da funksionallaşdırılır.
4 və 6-cı mövqelərin modikikasiyası orto-litiumlaşmanın köməyilə həyata keçirilir. Reaksiya şəraitindən asılı olaraq monolitium və dilitium törəmələrini almaq mümkündür: güclü qələvi mühitdə və tsikloheksanda qaynadıqda litiumlaşma iki dəfə baş verir, aşağı temperaturda isə mololitium törəməsi əmələ gəlir. Bundan əlavə, bu birləşmələr müəyyən elektrofillərlə reaksiyaya daxil edilir.
Mənbə
[redaktə | mənbəni redaktə et]- Benoit G. Dibenzothiophene (İngilis dili) // Üzvi Sintez üçün Reagentlərin Ensiklopediyası. — Wiley, 2014. — doi: 10.1002/047084289x.rn01695.
- Катализаторы гидроочистки 2017 / Солодова Н.Л., Нурмухаметова А.Р.
- Облагораживание тяжелого нефтяного сырья в чистой воде 2017 / Елецкий П.М., Соснин Г.А., Заикина О.О., Кукушкин Р.Г., Яковлев В.А.
- Современные процессы переработки угля 2009 / Николаева С. В., Латыпова Ф. Н., Шавшукова С. Ю.
- Гидрооблагораживание высокосернистых дизельных фракций 2015 / Лахова А.И., Петрова А.Н., Петров С.М., Баранов Д.В.
- Кинетические следствия образования серосодержащих соединений в процессе гидроочистки дизельной фракции нефти
- 2013 / Кривцова Надежда Игоревна, Иванчина Эмилия Дмитриевна, Занин Игорь Константинович, Ландл2ь Юлия Ивановна, Татаурщиков Антон Андреевич