Hidrogen rabitəsi
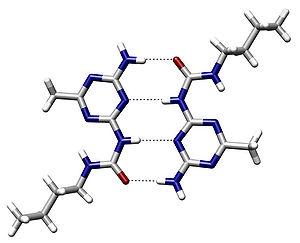
Hidrogen rabitəsi — oriyentasiya qüvvəsinin xüsusi növüdür. Flüor, oksigen və yaxud azot atomuna birləşmiş hidreogen atomu ilə flüor, oksigen və yaxud azot atomu arasında yaranan oriyentasiya qüvvəsinə hidrogen rabitəsi deyilir.
Hidrogen ionu[redaktə | mənbəni redaktə et]
hidrogen ionu (H+) heç bir elektronu olmayan və +1 yükə malik nüvədən ibarətdir. Buna görə onu bəzən "çılpaq" proton da adlandırırlar. Elektrona malik olmadığı üçün hidrogen ionunun müsbət yükü mənfi yüklü ionlar tərəfindən güclü surətdə cəzb olunur. Bununla əlaqədar olaraq, bir sıra molekullarda xüsusi təbiətə malik rabitə növü meydana çıxır ki, bu da bir qayda olaraq, hidrogenin iştirakı ilə əmələ gəldiyi üçün hidrogen rabitəsi adlanır.. h2o
İzahı[redaktə | mənbəni redaktə et]
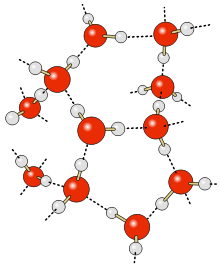
Hidrogen rabitəsi bilavasitə hidrogen ilə elektromənfiliyi yüksək olan elementlər (F,O,N və s.) arasında meydana çıxır. Məsələn, HF qaz halda polimerləşərək bir sıra polimerlər şəklində mövcud olur:H2F2, H3F3, H4F4, H5F5, H6F6 və s. Hidrogen rabitəsi adətən üç nöqtə ilə işarə edilir. Adi temperaturda H2O maye, H2S isə qazdır. halbuki bir sıra ümumi cəhətlərə əsasən bunun əksi müşahidə edilməlidir. Həmçinin suyun qaynama temperaturu (373oK) H2S-in qaynama temperaturundan (211oK) yüksəkdir. Bunlara səbəb H2S-dən fərqli olaraq, H2O molekulları arasında hidrogen rabitəsinin olmasıdır. Su molekulu iki hidrogen atomu və istifadə edilməmiş iki elektron cütünə malik olan bir oksigen atomundan ibarət olduğu üçün, o eyni vaxtda dörd hidrogen rabitəsi əmələ gətirə bilir. Burada elektron cütlərinin tetraedrik yerləşməsi ilə əlaqədar olaraq hidrogen rabitələri də fəzada həmçinin tetraedrik surətdə istiqamətlənir.
Suyu adətən H2O-nun dimerləri təşkil edir.
Təbiəti[redaktə | mənbəni redaktə et]
Hidrogen rabitəsi ion və kovalent rabitələrindən zəif, lakin Van-der-Vaals qüvvələrinə nisbətən davamlı rabitədir. Məsələn, ion və kovalent rabitələrə müvafiq gələn enerji təxminən 50-100 kkal/mol həddində olduğu halda, hidrogen rabitəsinin möhkəmliyi adətən 3-8 kkal/mol enerji ilə səciyyələnir. Lakin hidrogen rabitəsinin nisbətən zəif olmasına baxmayaraq, o maddələrin xassələrinin müəyyənləşməsinə əhəmiyyətli dərəcədə təsir göstərir. Digər tərəfdən bir çox hallarda həm molekullararası və həm də molekuldaxili hidrogen rabitəsi eyni vaxtda bir neçə yerdən əmələ gəlir. Bu da ümumiyyətlə hidrogen rabitəsinin möhkəmliyinin artmasına səbəb olur.
Hidrogen rabitəsi polimer birləşmələrdə[redaktə | mənbəni redaktə et]
Hidrogen rabitəsi süni və təbii polimer birləşmələrinin kimyasında böyük əhəmiyyət kəsb edir. Məsələn, sellüloza molekullarının öz aralarında birləşərək lif əmələ gətirməsi bilavasitə hidrogen rabitəsinə əsaslanır.
Bioloji rolu[redaktə | mənbəni redaktə et]
Hidrogen rabitəsinin böyük bioloji rolu da müəyyən edilmişdir. irsiyyət məsələlərində dezoksiribonukleun turşuları başlıca rol oynayır. Bu turşulara məxsus xüsusi quruluş isə orada hidrogen pabitələrinin olması ilə əlaqədardır.
Mənbə[redaktə | mənbəni redaktə et]
- Z.Qarayev "Qeyri-üzvi kimya", Maarif-1975.
- Химическая Энциклопедия. Советская Энциклопедия. — М., 1988.
- В. В. Москва. Водородная связь в органической химии. Соросовский образовательный журнал, 11999,N 2, с.58-64 [3]
- Пиментел Дж., О. Мак-Клеллан. Водородная связь, пер. с англ.. — М., 1964.
- Эпштейн Л.М, Шубина Е.С. Многоликая водородная связь // «Природа». — 2003. — № 1.
- Водородная связь. Сб. ст.. — М., 1964.
- Pauling L. The chemical bond. — N. Y., 1967.

