Kapsid


Kapsid — genetik materialını ehtiva edən virusun zülal zərfidir. Protomerlər deyilən bir neçə oliqomerik (təkrarlanan) struktur alt hissədən ibarətdir. Fərdi zülallara uyğun gələn və ya uyğun gəlməyən müşahidə edilən üç ölçülü morfoloji alt birləşmələrə kapsomerlər deyilir. Kapsidi təşkil edən zülallara kapsid zülalları və ya viral zərf zülalları (VCP) deyilir. Kapsid və daxili genoma nukleokapsid deyilir[2][3][4] .
Kapsidlər quruluşlarına görə geniş şəkildə təsnif edilir. Əksər viruslarda zəncir və ya ikozahedral kapsid var. Bakteriofaqlardakı kimi bəzi viruslar elastiklik və elektrostatik məhdudiyyətləri səbəbindən daha mürəkkəb quruluşlar inkişaf etdirmişdir. 20 bərabər tərəfli üçbucaqlı üzə sahib olan icosahedronun forması bir kürəyə yaxınlaşır, spiral forması isə bir silindr boşluğunu tutur, lakin silindrin özü deyil, yay şəklini xatırladır. Kapsid kənarları bir və ya daha çox zülaldan ibarət ola bilər. Məsələn, FMD virusu kapsidinin VP1-3 adlanan üç cəhəti var[5] [6].
Bəzi viruslar əhatə olunur, yəni kapsidin viral zərf olaraq bilinən bir lipid membranı ilə örtülməsi deməkdir. Zərf kapsid tərəfindən virusun sahibinin hüceyrədaxili membranından alınır; nümunələrə daxili nüvə membranı, Golgi membranı və xarici hüceyrə membranı daxildirv[7] .
Virus hüceyrəyə yoluxduqdan və təkrarlanmağa başladıqdan sonra hüceyrənin protein biosintezi mexanizmindən istifadə edərək yeni kapsid alt birləşmələri sintez olunur. Spiral kapsidli və xüsusilə RNT genomlu olanlar da daxil olmaqla bəzi viruslarda kapsid zülalları genomları ilə birlikdə birləşdirilir. Digər viruslarda, xüsusən də cüt zolaqlı DNT genomlu daha mürəkkəb viruslarda, kapsid zülalları, bir təpədə ixtisaslaşmış bir portal quruluşunu ehtiva edən boş prokapsid progenitorlara birləşir. Bu portal vasitəsi ilə viral DNT kapsidə gedir[8][9].
Virusları klonlara təsnif etmək üçün əsas kapsid zülalı (MCP) arxitekturasının struktur analizindən istifadə edilmişdir. Məsələn, bakteriofaq PRD1, yosun virusu Paramekium bursaria Chlorella virusu (PBCV-1), mimivirus və məməlilərin adenovirusu eyni nəslə, quyruq ikiqat telli DNT (Kaudovirales) və herpes virusu olan bakteriyofaqlar ikinci sıraya aid edilmişdir[10][11][12][13] .
Xüsusi formalar
[redaktə | mənbəni redaktə et]

İkosaedral
[redaktə | mənbəni redaktə et]İkosaedral quruluşu viruslar arasında son dərəcə yayılmışdır[14]. ,İkosaedron 12 deşikli zirvələrlə ayrılmış 20 üçbucaqlı üzdən ibarətdir və 60 asimmetrik vahiddən ibarətdir[15]. Beləliklə, ikosahedral virus 60N protein alt birliyindən ibarətdir. Kapsomerlərin ikosaedral kapsiddəki sayı və yeri Donald Kaspar və Aaron Klaq tərəfindən təklif olunan “kvazi ekvivalentlik prinsipi” istifadə edilərək təsnif edilə bilər. Quruluşu pentamerin kənarından h addım ataraq saat yönünün əksinə 60 dərəcə çevirərək, sonrakı pentamerə keçmək üçün k addım ataraq düşünmək olar. Kapsid üçün trianqulyasiya sayı T aşağıdakı kimi təyin olunur[16] :
Bu sxemdə ikosaedral kapsidlər 12 pentamer üstəgəl 10 (T - 1) hexamer ehtiva edir. T rəqəmi kapsidlərin ölçüsünü və mürəkkəbliyini təmsil edir. [ , k və T-nin bir çox dəyərləri üçün həndəsi nümunələrə Geodeziya və Goldberg Poltopes Siyahısında rast gəlmək olar[17].
Bu qaydanın bir çox istisnası var: məsələn, poliavaviruslar və papillomaviruslarda kvazi-T = 7 qəfəsdə altıbucaqlı mövqedə hexamer əvəzinə pentamerlər vardır.Reovirus, rotavirus və bakteriofaq inkludinq daxil olmaqla ikili zəncirli RNT virus xəttinin üzvləri 120 nüsxə kapsiddən ibarət olan "T = 2" kapsidinə uyğun bir zülal və ya asimmetrik bölgədə dimer olan bir T = 1 kapsiddən ibarət kapsidlərə sahibdirlər. Blok. Eynilə, bir çox kiçik viruslarda T = 3 qəfəsə görə düzəldilmiş, ancaq üç yarı ekvivalent mövqe tutan fərdi polipeptidlərlə yalançı T = 3 (və ya P = 3) kapsid var[18] .
T nömrələri müxtəlif yollarla təmsil oluna bilər, məsələn, T = 1 yalnız bir ikosaedr və ya dodekaedr kimi, kvazi simmetriya növündən asılı olaraq T = 3 isə kəsilmiş bir dodekahedron, ikosododekaedron, və ya kəsilmiş bir ikosaedron və onlara uyğun əkizlər - , rombik triacontahedron və ya pentakis-dodekaedron.[19]
Uzatmaq
[redaktə | mənbəni redaktə et]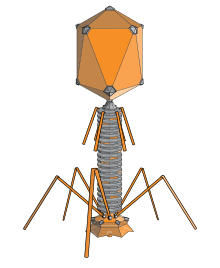
Uzanan bir ikosaedron, bakteriyofaq başlarının yayılmış bir formasıdır. Bu dizayn hər iki ucunda qapaqları olan bir silindrdən ibarətdir. Silindr 10 uzanan üçbucaq üzdən ibarətdir. Hər hansı bir müsbət tam sayı ola bilən Q (və ya Tmid) rəqəmi, silindrin 10 üçbucağını təşkil edən asimmetrik altüçbucaqlarının sayını təyin edir[20]. E.coli uzanan T4 bakteriyofajının sahibidir. Bakteriyofaq tərəfindən şifrələnmiş gp31 proteini, E. coli şaparon proteini GroES üçün funksional olaraq homoloqdur və infeksiya zamanı bakteriofaq T4 virionlarının yığılması zamanı onu əvəz edə bilir[21] .
Spiral
[redaktə | mənbəni redaktə et]Bir çox çubuq formalı və filamentli bitki viruslarında spiral simmetriyalı kapsidlər olur[22] [23] . Spiral çevrilmələr iki kateqoriyaya bölünür: bir ölçülü və iki ölçülü spiral sistemlər. Bütün zəncir quruluşun yaradılması bir zülal məlumat bankında kodlanmış bir sıra tərcümə və fırlanma matrislərinə əsaslanır. Spiral simmetriya P = μ x ρ düsturu ilə verilir, burada μ - spiralın bir döngəsindəki struktur vahidlərinin sayı, ρ - vahid başına eksenel qaldırıcı və P - spiralın pitchidir. Spiralın uzunluğunu dəyişdirərək istənilən həcmin bağlana bilməsi səbəbindən quruluşa açıq deyilir. Ən yaxşı öyrənilmiş spiral virus tütün mozaika virusudur. Virus tək bir molekul (+) RNT zənciridir. Zəncirin içindəki hər bir zərf zülalı, RNT genomunun üç nükleotidini birləşdirir. A qripi virusları bir neçə ribonükleoprotein ehtiva etmələri ilə fərqlənir, viral NP zülalı RNT-ni sarmal bir quruluş halına gətirir. Ölçü də fərqlidir; tütün mozaika virusu zəncirin hər döngəsində 16.33 protein alt birliyi ehtiva edir , qrip A virusu isə 28 amin turşusundan ibarət quyruq halqasına malikdir[24].
Funksiyalar
[redaktə | mənbəni redaktə et]
Kapsid funksiyaları:
- genomu qorumaq,
- genomu çatdırmaq və
- sahibi ilə qarşılıqlı əlaqə qurmaq[25] .
Genomu ölümcül kimyəvi və fiziki təsirlərdən qorumaq üçün virus sabit bir qoruyucu protein qatını yığmalıdır[26]. Bunlara təbii olaraq meydana gələn radiasiya formaları, həddindən artıq pH və ya temperatur və proteolitik və nükleolitik fermentlər daxildir. Zərfsiz viruslar üçün kapsid özü, hüceyrə hüceyrəsindəki reseptorlarla qarşılıqlı təsir göstərə bilər ki, bu da hüceyrə hüceyrə membranından nüfuz etməyə və kapsidin içərisinə keçməsinə səbəb olur. Genomun çatdırılması sonradan kapsidin soyulması və ya sökülməsi və genomun sitoplazmaya salınması ilə və ya genomun xüsusi bir portal quruluşu vasitəsi ilə birbaşa ev sahibi hücrenin nüvəsinə atılması ilə baş verir.
Mənşəyi və təkamülü
[redaktə | mənbəni redaktə et]Bir çox viral kapsid zülalının funksional cəhətdən müxtəlif hüceyrə zülallarından təkrarən inkişaf etdiyi irəli sürülmüşdür. Hüceyrə zülallarının işə götürülməsi təkamülün müxtəlif mərhələlərində baş vermiş kimi görünür, buna görə bəzi hüceyrə zülalları həyatın üç müasir bölgəsindəki hüceyrə orqanizmlərinin fərqliliyindən əvvəl tutuldu və yenidən işlək vəziyyətə gəldi, digərləri isə nisbətən yaxın zamanda tutuldu. Nəticədə, bəzi kapsid zülalları uzaqdan əlaqəli orqanizmlərə yoluxan viruslarda geniş yayılmışdır , digərləri isə müəyyən bir virus qrupu ilə məhdudlaşır .
Bir hesablama modeli , kapsidlərin viruslardan əvvəl yarana bildiyini və replikator cəmiyyətləri arasında üfüqi bir köçürmə vasitəsi kimi xidmət etdiyini göstərdi, çünki gen parazitlərinin sayı artarsa bu cəmiyyətlər yaşaya bilməz və müəyyən genlər meydana gəlmədən məsuldur. bu quruluşların və özünü çoxaldan icmaların sağ qalmasına kömək edənlərin. Bu irsi genlərin hüceyrəli orqanizmlər arasındakı yerdəyişməsi təkamül prosesində yeni virusların yaranmasına səbəb ola bilər[27].
İstinadlar
[redaktə | mənbəni redaktə et]- ↑ Asensio MA, Morella NM, Jakobson CM, Hartman EC, Glasgow JE, Sankaran B, və b. "A Selection for Assembly Reveals That a Single Amino Acid Mutant of the Bacteriophage MS2 Coat Protein Forms a Smaller Virus-like Particle". Nano Letters. 16 (9). September 2016: 5944–50. Bibcode:2016NanoL..16.5944A. doi:10.1021/acs.nanolett.6b02948. PMID 27549001. 2021-12-03 tarixində arxivləşdirilib. İstifadə tarixi: 2021-06-21.
- ↑ Asensio MA, Morella NM, Jakobson CM, Hartman EC, Glasgow JE, Sankaran B, və b. "A Selection for Assembly Reveals That a Single Amino Acid Mutant of the Bacteriophage MS2 Coat Protein Forms a Smaller Virus-like Particle". Nano Letters. 16 (9). September 2016: 5944–50. Bibcode:2016NanoL..16.5944A. doi:10.1021/acs.nanolett.6b02948. PMID 27549001. 2021-12-03 tarixində arxivləşdirilib. İstifadə tarixi: 2021-06-21.
- ↑ Lidmar J, Mirny L, Nelson DR. "Virus shapes and buckling transitions in spherical shells". Physical Review E. 68 (5 Pt 1). November 2003: 051910. arXiv:cond-mat/0306741. Bibcode:2003PhRvE..68e1910L. doi:10.1103/PhysRevE.68.051910. PMID 14682823.
- ↑ Vernizzi G, Olvera de la Cruz M. "Faceting ionic shells into icosahedra via electrostatics". Proceedings of the National Academy of Sciences of the United States of America. 104 (47). November 2007: 18382–6. Bibcode:2007PNAS..10418382V. doi:10.1073/pnas.0703431104. PMC 2141786. PMID 18003933.
- ↑ Vernizzi G, Sknepnek R, Olvera de la Cruz M. "Platonic and Archimedean geometries in multicomponent elastic membranes". Proceedings of the National Academy of Sciences of the United States of America. 108 (11). March 2011: 4292–6. Bibcode:2011PNAS..108.4292V. doi:10.1073/pnas.1012872108. PMC 3060260. PMID 21368184.
- ↑ Branden, Carl; Tooze, John. Introduction to Protein Structure. New York: Garland. 1991. 161–162. ISBN 978-0-8153-0270-4.
- ↑ "Virus Structure (web-books.com)". 2021-02-07 tarixində arxivləşdirilib. İstifadə tarixi: 2021-06-21.
- ↑ Alberts, Bruce; Bray, Dennis; Lewis, Julian; Raff, Martin; Roberts, Keith; Watson, James D. Molecular Biology of the Cell (4th). 1994. səh. 280.
- ↑ Newcomb WW, Homa FL, Brown JC. "Involvement of the portal at an early step in herpes simplex virus capsid assembly". Journal of Virology. 79 (16). August 2005: 10540–6. doi:10.1128/JVI.79.16.10540-10546.2005. PMC 1182615. PMID 16051846.
- ↑ Krupovic M, Bamford DH. "Virus evolution: how far does the double beta-barrel viral lineage extend?". Nature Reviews. Microbiology. 6 (12). December 2008: 941–8. doi:10.1038/nrmicro2033. PMID 19008892.
- ↑ Forterre P. "Three RNA cells for ribosomal lineages and three DNA viruses to replicate their genomes: a hypothesis for the origin of cellular domain". Proceedings of the National Academy of Sciences of the United States of America. 103 (10). March 2006: 3669–74. Bibcode:2006PNAS..103.3669F. doi:10.1073/pnas.0510333103. PMC 1450140. PMID 16505372.
- ↑ Khayat R, Tang L, Larson ET, Lawrence CM, Young M, Johnson JE. "Structure of an archaeal virus capsid protein reveals a common ancestry to eukaryotic and bacterial viruses". Proceedings of the National Academy of Sciences of the United States of America. 102 (52). December 2005: 18944–9. doi:10.1073/pnas.0506383102. PMC 1323162. PMID 16357204.
- ↑ Laurinmäki PA, Huiskonen JT, Bamford DH, Butcher SJ. "Membrane proteins modulate the bilayer curvature in the bacterial virus Bam35". Structure. 13 (12). December 2005: 1819–28. doi:10.1016/j.str.2005.08.020. PMID 16338410.
- ↑ Caspar DL, Klug A. "Physical principles in the construction of regular viruses". Cold Spring Harbor Symposia on Quantitative Biology. 27. 1962: 1–24. doi:10.1101/sqb.1962.027.001.005. PMID 14019094.
- ↑ Carrillo-Tripp M, Shepherd CM, Borelli IA, Venkataraman S, Lander G, Natarajan P, və b. "VIPERdb2: an enhanced and web API enabled relational database for structural virology". Nucleic Acids Research. 37 (Database issue). January 2009: D436–42. doi:10.1093/nar/gkn840. PMC 2686430. PMID 18981051. 2018-02-11 tarixində orijinalından arxivləşdirilib. İstifadə tarixi: 2021-06-21.
- ↑ Johnson JE, Speir JA. Desk Encyclopedia of General Virology. Boston: Academic Press. 2009. 115–123. ISBN 978-0-12-375146-1.
- ↑ Mannige RV, Brooks CL. "Periodic table of virus capsids: implications for natural selection and design". PLOS ONE. 5 (3). March 2010: e9423. Bibcode:2010PLoSO...5.9423M. doi:10.1371/journal.pone.0009423. PMC 2831995. PMID 20209096.
- ↑ Sgro, Jean-Yves. "Virusworld". Institute for Molecular Virology. University of Wisconsin-Madison. 2022-01-20 tarixində arxivləşdirilib. İstifadə tarixi: 2021-06-21.
- ↑ Damodaran KV, Reddy VS, Johnson JE, Brooks CL. "A general method to quantify quasi-equivalence in icosahedral viruses". Journal of Molecular Biology. 324 (4). December 2002: 723–37. doi:10.1016/S0022-2836(02)01138-5. PMID 12460573.
- ↑ Luque A, Reguera D. "The structure of elongated viral capsids". Biophysical Journal. 98 (12). June 2010: 2993–3003. Bibcode:2010BpJ....98.2993L. doi:10.1016/j.bpj.2010.02.051. PMC 2884239. PMID 20550912.
- ↑ Marusich EI, Kurochkina LP, Mesyanzhinov VV. Chaperones in bacteriophage T4 assembly. Biochemistry (Mosc). 1998;63(4):399-406
- ↑ Yamada S, Matsuzawa T, Yamada K, Yoshioka S, Ono S, Hishinuma T. "Modified inversion recovery method for nuclear magnetic resonance imaging". The Science Reports of the Research Institutes, Tohoku University. Ser. C, Medicine. Tohoku Daigaku. 33 (1–4). December 1986: 9–15. PMID 3629216.
- ↑ Aldrich RA. "Children in cities--Seattle's KidsPlace program". Acta Paediatrica Japonica. 29 (1). February 1987: 84–90. doi:10.1111/j.1442-200x.1987.tb00013.x. PMID 3144854.
- ↑ Ye Q, Guu TS, Mata DA, Kuo RL, Smith B, Krug RM, Tao YJ. "Biochemical and structural evidence in support of a coherent model for the formation of the double-helical influenza A virus ribonucleoprotein". mBio. 4 (1). 26 December 2012: e00467–12. doi:10.1128/mBio.00467-12. PMC 3531806. PMID 23269829.
- ↑ Krupovic M, Koonin EV. "Multiple origins of viral capsid proteins from cellular ancestors". Proceedings of the National Academy of Sciences of the United States of America. 114 (12). March 2017: E2401–E2410. doi:10.1073/pnas.1621061114. PMC 5373398. PMID 28265094.
- ↑ Jalasvuori M, Mattila S, Hoikkala V. "Chasing the Origin of Viruses: Capsid-Forming Genes as a Life-Saving Preadaptation within a Community of Early Replicators". PLOS ONE. 10 (5). 2015: e0126094. Bibcode:2015PLoSO..1026094J. doi:10.1371/journal.pone.0126094. PMC 4425637. PMID 25955384.
- ↑ Krupovic M, Dolja VV, Koonin EV. "Origin of viruses: primordial replicators recruiting capsids from hosts" (PDF). Nature Reviews. Microbiology. 17 (7). July 2019: 449–458. doi:10.1038/s41579-019-0205-6. PMID 31142823. 2022-03-28 tarixində arxivləşdirilib (PDF). İstifadə tarixi: 2021-06-21.
