Kimya
| Kimya | |||||||
 | |||||||
| Elm sahəsi → öyrənir | |||||||
|---|---|---|---|---|---|---|---|
| Yarımbölmə → öyrənir | |||||||
| |||||||
Kimya – maddənin tərkibini, quruluşunu, xassələrini ,çevrilməsini və bu çevrilmələr zamanı baş verən hadisələri öyrənən təbiət elmidir.[1] Kimyanın mühüm vəzifələrinə zəruri maddələrin alınması, maddələrin çevrilməsini və bu çevrilmələri müşahidə edən hadisələri öyrənmək, ətraf mühtin mühafizəsi və s. kimi vəzifələr aiddir.[2]
Etimologiyası
[redaktə | mənbəni redaktə et]Kimya sözünün nə vaxt meydana gəlməsi və ilk olaraq hansı mənanı ifadə etməsini dəqiq müəyyənləşdirmək mümkün deyil. Bir çox kimya tarixçiləri öz hipotezlərini təklif etsələr də, vahid bir fikir formalaşmadı. XVII əsrin başlanğıcından "kimya", "kimyaçı" məfhumları elmi ədəbiyyata, monoqrafiyalara və dərsliklərə möhkəm surətdə daxil oldu. Müxtəlif avropa dillərində "kimya" sözü oxşar səslənməyə malikdir: ing. chemistry, alm. chemie, çex və hollandca chemic, fransızca və rumın dilində chimie, italyanca chimica, polyak, slovak və latın dillərində chemia, litva dilində chemija, ispan və portuqal dillərində quimica, İsveç dilində kemi, eson dilində keemia, xorvat və sloven dillərində kemija, latış dilində kimija, Norveç dilində kjeıııi adlanır. Əgər fikir versək, bütün sözlərdə "kem" və ya "kim" kökləri vardır. Tarixçilərin bir neçəsi qeyd edir ki, "kimya" sözü qədim yunan dilinin bir neçə sözü ilə həmahəngdir. Məs., təbabət və əczaçılığa dair əlyazmalarda rast gəlinən "kimos" və ya "kümos" sözləri "sərbəst" mənasını verirdi. "Kima" və ya "küna" sözləri isə "tökmə" kimi tərcümə olunurdu. Məntiqi nəticə kimi ehtimal etmək olar ki, ilk əvvəllər "kimya", "metalların əridilməsi və tökməsi sənəti" idi. "Kimevsis" sözünün mənası isə "qarışdırma"dır ki, bu əməliyyat da bir çox kimyəvi proseslərdə geniş istifadə olunur. Belə ki, "ximevsis" sözü də tam hüquqla "kimya" sözünün sələfi ola bilər.[3]
Tarix
[redaktə | mənbəni redaktə et]Kimya elmi inkişaf dövründə 4 əsas mərhələdən keçmişdir:[4]
Əlkimyadan əvvəlki dövr (Qədim Misir)
[redaktə | mənbəni redaktə et]Kimyanın bilinən tarixi Qədim Misir dövründə başlamışdır. E.ə. 2000-ci illərdə Misirlilərin kimyəvi üsullar istifadə edərək kosmetik tozlar çıxardıqları iddia edilməkdədir. Kral Hammurapi dövründə (e.ə 1792–1750) Babillər qızıl, gümüş, civə, güllə, dəmir və mis kimi metalları təyin olunmuş və bu metallara simvollar verilmişdir. Erkən Yunan fəlsəfəçilər (Sokrat əvvəli mütəfəkkirlər) təbii hadisələri fövqəltəbii olmayan səbəblərlə şərhə çalışmışlar, bunun nəticəsində də bu dövrdə əlkimya əvvəli kimya elminin təməlləri atılmışdır. Miletli Tales (e.ə 624 – e.ə 546) maddənin prinsiplərini araşdırmış və suyun kainatın təməl maddəsi olduğunu önə sürmüşdür. Bir başqa Miletli Anaksimandros (e.ə 610- e.ə 546) suyun əleyhdarı olan atəşin necə meydana gəldiyini sorğulamışdır. Empedokles (e.ə 490–430) kainatın 4 təməl element atəş, hava, su və torpaqdan meydana gəldiyini iddia etmişdir. Empedoklesin tərifinə görə torpaq bərk/qatı maddələri, su maye maddələri və metalları, hava qazları ifadə etməkdə idi. Bununla birlikdə atəşi də bir müddətdən çox maye, qaz və bərk/qatı kimi maddənin bir halı olaraq təyin etmişdir. Demokritosun müəllimi Leukippos kainatın iki növ elementdən meydana gəldiyini (boşluq və bərk/qatı) ifadə etmiş, boşluğun və qatılığın kainatdakı bütün elementləri meydana gətirdiyini ifadə etmişdir. Democritus (e.ə 460–370 ) Leukippos ilə birlikdə atomçu nəzəriyyəni inkişaf etdirmişdir. Maddələrin quruluş daşı olaraq daha kiçik parçalara ayrıla bilməyən atomlar Leucippus və Democritusun inkişaf etdirdiyi bir fəlsəfə sistemi olaraq qəbul edilməsinə baxmayaraq Platon bu atomçuluq nəzəriyyəsinə bölünə bilməzlik prinsipini əlavə etmişdir. Platon kainatı meydana gətirən 4 təməl elementin geometrik qatılardan meydana gəldiyini bu qatılarında üçbucaq səthlərdən meydana gəldiyini iddia etmişdir. Aristotel (e.ə 384–323) elementlərin xüsusiyyətləri düşüncəsini təyin etdirmişdir. Fərqli elementlərin fərqli xüsusiyyətləri olduğunu və bunun müxtəlif dəyişənlərə bağlı olduğunu ifadə etmişdir. Bu xüsusiyyətləri dəyişdirildiyində bir elementin başqa bir elementə çevrilə biləcəyini və maddələrin dəyişmə halında olduğunu iddia etmişdir.
Əlkimya(kimyagərlik) dövrü
[redaktə | mənbəni redaktə et]Kimya, tarixi olaraq kimyagərlikdən ayrılaraq ortaya çıxmışdır. Kimyanın yaranmasına qədər keçən minlərlə il boyunca maddələrin xüsusiyyətləriylə və bir-birləriylə olan qarşılıqlı təsirləri ilə maraqlananlar kimyagərlər olmuşdur. Eynilə günümüz kimyaçıları kimi kimyagərlər də zamanlarının böyük bir hissəsini laboratoriyalarında keçirərdi. Amma onlar, kimyaçılar kimi maddələr arasındakı əlaqələrin necə olduğunu, dəyişmələrin niyə ortaya çıxdığını anlamağa çalışmazdı. Kimyagərlər başlıca məşğuliyyəti, sıravi maddələri daha qiymətli maddələrə çevirmənin yollarını tapmaq idi. Hər kimyagərin xülyalarını bəzəyən maddələrin başında da "fəlsəfə daşı" (ya da "fəlsəfəçi daşı") olaraq bilinən, cadulu bir daşı əldə etmək gəlirdi. Bu daşın, daşıdığı güc sayəsində mis, qalay, dəmir ya da güllə kimi sıravi metalları altına çevirdiyinə inanılardı. Bunun yanında bəzi kimyagərlər də həyatlarını hər cür xəstəliyi yaxşılaşdırdığına, sonsuz gənclik və ölümsüzlük verdiyinə inanılan ‘həyat sununu (əl iksir ya da ABi həyat) axtarışa həsr etmişdi. Çindən Hindistana, Orta şərqdən Avropaya qədər bütün kimyagərlərin başlıca çalışdıqları bunlar idi. Kimyagərlərlə məşğul olanların təbiətə və onu meydana gətirən maddələrə baxışları çox fərqli idi. Onların da özlərinə xas amma elmi olmayan bəzi qaydaları vardı. Məsələn dörd təməl elementə inanardılar. Bunlar hava, torpaq, atəş və su idi. Onlara görə yer üzündəki bütün maddələr bu dörd təməl elementin dəyişik nisbətlərdəki qarışığından meydana gəlmişdi. Bunun yanında bu elementlərin daşıdığı bəzi təməl xüsusiyyətlər də vardı: soyuqluq, quruluq, istilik və yaşlıq. Hər element bu dörd təməl xüsusiyyətdən ikisini daşıyardı. Atəş istilik və quruluq özəlliklərini daşıyardı. Torpaq quru və soyuq idi; hava isti və yaş idi; su da yaş və soyuq idi.Şübhəsiz Kimyagərliyin fəlsəfə daşını ya da həyat sununu əldə etmək üçün sınadığı heç bir üsul nəticə vermədi. Amma minlərlə il boyunca minlərlə kimyagərin bu korkoranə səyi əsnasında insanların faydasına bir çox maddə tapıldı, müxtəlif alətlər inkişaf etdirildi və üsullar ortaya çıxdı. Təbiətin gerçək element olan elementlərə bağlı böyük bir məlumat təcrübəsi meydana gəldi. Müasir kimyanın təməlləri yavaş yavaş atıldı. Zamanla kimyagərliyin cadu əsaslı boş inanışları, təsirini itirməyə başladı. Kimyagər işləri 1400-cü illərdə doruğa çatdıqdan sonra insanlar kimyagər qaydalarına olan inanclarını itirməyə başladılar. Xüsusilə İntibahla birlikdə təbiəti anlamaq üçün diqqətli müşahidələr aparan, diqqətli ölçümlər və bəzi təcrübələr edən bəzi insanlar ortaya çıxdı. Bunlar işlərində cadu ya da simyaya müraciət etmirdi. Bu cür işlər gedərək yayıldı, mətbəə sayəsində də kitablarla paylaşılmağa və yaxşıca yayılmağa başladı. Hər şeyə baxmayaraq kimyagərlik 1600-cü illərin sonuna qədər kimyayla birlikdə varlığını davam etdirdi. Bir çox elm insanı təbiəti və insanı elmi olaraq ələ almadan əvvəl bir müddət kimyagərliklə məşğul oldu. Kimyagərlər, Fəlsəfə Daşı deyilən bir daşın, metalları qızıla çevirmə gücü olduğuna inanardı. Bir çox kimyagərlərin təməl məqsədi sıravi metallardan qızıl əldə etmək idi. Bunun üçün bir sıra başqa təcrübələr etməkdən çəkinmirdilər. Məsələn Hamburglu kimyagər Henrig Brand bu məqsədlə 1669 tarixində aslan sidiyi ilə yüzlərlə təcrübə etmişdi. Ona görə bu soylu heyvanın sidiyində qızıl olmalı idi. Brand aylar sürən səyinin sonunda şübhəsiz qızıl əldə edə bilmədi amma parlayan yeni bir maddə tapdı. Ona ‘işıq daşıyan' mənasını verən Yunanca ‘fosfor' adını verdi.
Ənənəvi kimya
[redaktə | mənbəni redaktə et]Bu dövr XVII əsr sonuyla XIX əsr başlarına bərabər gəlməkdədir. Johann Joachim Becher XVII əsr ortalarında yanma ilə əlaqədar Phlogiston nəzəriyyəsini inkişaf etdirmişdir. Bu nəzəriyyəyə görə hər yanıcı maddə phlogiston deyə adlandırılan qoxusuz, rəngsiz, dadsız və ağırlıqsız bir məzmun ehtiva etməkdə idi və bu məzmun yanma reallaşdığında yanıcı maddə tərəfindən mühitə salınmaqda idi. Bu nəzəriyyə daha sonra Georg Ernst Stahl tərəfindən daha məşhur bir hala gətirilmiş XVIII əsrin böyük bir qisimində ümumi qəbul görmüşdür. 1785–1787 illəri arasında Fransız fizikaçı Çarlz Augustine də indiki vaxtda Coulomb qanunu olaraq adlandırılan bənzər yüklü maddələrin bir-birini itələdiyi əleyhdar yüklülərin bir-birini çəkdiyi və bu çəkiliş ya da itələnən qüvvətinin hesablanması üçün lazımlı tənliyi də ehtiva edən qanunu tapmışdır. Phlogiston nəzəriyyəsi XVIII əsrin sonlarına gəlindiyində Lavoisier tərəfindən yürüdülmüşdür. Daha əvvəldən Phlogiston nəzəriyyəsinə görə də, phlogiston maddəsi olaraq adlandıralan maddənin oksigen olduğunu kəşf etmişdir. 1803-cü ildə John Dalton atom nəzəriyyəsini royal institutunda ilk dəfə təqdim etmişdir. Bu nəzəriyyəyə görə fərqli elementlərin atomları, fərqli ağırlıqlara sahibdirlər. Bu nəzəriyyənin bəzi qanunları aşağıdakılardır:
- Bütün maddələrr atomlardan ibarətdir.
- Atomlar daha kiçik hissələrə parçalana bilməzlər.
- Eyni elementin bütün atomları bir-birinin eynisidir.
- Fərqli elementlər fərqli atomlara malikdir.
- Atomların yenidən təşkil edilməsi nəticəsi kimyəvi reaksiyalar meydana gəlir.
- Birləşmələr elementlərdən təşkil olunub.
Bu nəzəriyyə ilə müasir kimyanın təməlləri qoyulmuşdur.
Müasir kimya
[redaktə | mənbəni redaktə et]Bu dövr XIX əsr və sonrasını əhatə edir. Heinrich Geibler (1814–1879) 1854-cü ildə suyun ən yüksək sıxlığa 3.8 C° çatdığını öz icad etdiyi bir mexanizmlə göstərmişdir (daha sonra bu istiliyin 3.98 C° olduğu tapılmışdır). Daha sonra isə Geisslerin icad etdiyi vakuum balonuyla William Crookes atom nəzəriyyəsində irəliləmələr qeyd etmiş və Cathode relsi kəşf etmişdir. Eugen Qoldsteinin (1850–1930) işləri protonun varlığını isbat etmişdir. C.C.Tomson (1856–1940) öz atom modelini inkişaf etdirmiş və 1906-cı ildə Nobel fizika mükafatını qazanmışdır. Mendeleyev dövri cədvəli 1869-cu ildə Kimyanın Prinsipləri əsərində nümayiş etmişdir. Bu dövri cədvəldə bilinən 63 elementi atom ağırlıqlarına və bənzər xüsusiyyətlərinə görə sıralamışdır. Mariya Küri (1867–1934) radioaktivliyi və sonrasında Polonium və Radiumu kəşf etmiş və 1911-ci ildə Nobel kimya mükafatını qazanmışdır. Ernest Rutherford 3 növ radioaktivliyi alfa hissəciyi (+), beta hissəciyi (-) və qamma şüasını kəşf etmişdir. Bu inkişafların sonrasında və əvvəlində daha bir çox elm insanının töhfəsilə kimya elmi günümüzə çatmışdır. 2011-ci il Birləşmiş Millətlər tərəfindən beynəlxalq kimya ili elan edilmişdir.[5] Nüvə reaksiyaları yolu ilə Dubna və Kaliforniyada ifrat ağır elementlərin alınmışdır.Elementlərin ikinci yüzlüyü Md ilə başlamışdır.Hal hazırda Rentgenium,Kopernikium,Flörovium,Ununtrium,Tenessinium,Flörovium,Ununoktium (Oqaneson) və Ununennium alınmışdır.
Qədim kimyaçılar əlkimyaçılar adlanır.Misir torpaqları qara torpaq olduğu üçün Kimya sözü Xemiya Şablon:Qara torpaq sözündən götürülmüşdür.
Kimyanın əsas anlayışları
[redaktə | mənbəni redaktə et]Kimyanın tədqiqat obyekti maddələr – atom və molekullardır. Bunlar kimyəvi hissəciklər adlanırlar. Onların ölçüsü 10−10 – 10−6 metr arasında olur. Bundan kiçik ölçülü hissəcikləri fizika öyrənir. Həmin hissəciklər mikrohissəciklər adlanır. Ölçüsü iri olan hissəciklərdə baş verən prosesləri də fizika öyrənir.
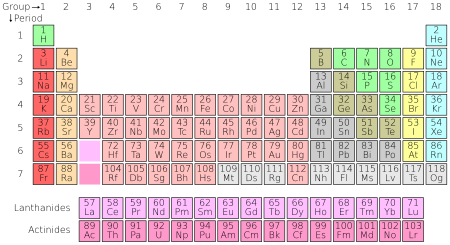
Adi kimyəvi üsullarla daha bəsit maddələrə ayırmanın mümkün olmadığı təbii və süni maddələr. Kimyəvi elementlər bir-biri ilə birləşərək bizi əhatə edən aləmin bütün mürəkkəb maddələrini əmələ gətirir. Hər kimyəvi, nüvəsində eyni sayda elektrik yükü və atom örtüyündə eyni sayda elektron olan atomlardan yaranmışdır. Atomların nüvəsi sayca həmin elementin atom nömrəsinə bərabər protondan və müxtəlif sayda neytrondan ibarətdir. Eyni elementin kütlə ədədləri müxtəlif olan növlərinə izotop deyilir. Kimyəvi elementlərin çoxunun təbiətdə iki və ya daha artıq izotopu var. 81 elementin 276 sabit və 1500-ə yaxın radioaktiv izotopu məlumdur. Yer üzərində təbii elementlərin izotop tərkibi, adətən, sabit olduğundan hər elementin atom kütləsi, demək olar ki, daim sabit qalır və elementin ən mühüm xarakteristikalarından biridir.
Hələlik elmə məlum olan Kimyəvi elementlərin sayı 176-dır (2017).Bu elementlərin 118 -i stabil nuklidlərdir.Və bu elementlərin 118-i" İUPAK" tərəfindən adlandırılmışdır.Onların əksəriyyəti radioaktiv deyil və təbiətdə mövcud olan bütün bəsit və mürəkkəb maddələri əmələ gətirir. Bəsit maddə — elementin sərbəst haldakı formasıdır.Bu o deməkdir ki, elementlər birləşib bir və ya bir neçə bəsit maddə əmələ gətirir.Bu hadisə allotropiya adlanır.Allotropiya iki səbəbdən baş verə bilər. I.Kristal quruluşda olan müxtəliflik. II.Molekulda olan atomların sayının müxtəlifliyi. Oksigendə allotropiya 2 səbəbə görə ancaq fosforda isə 1 səbəbə görə baş verir.
Məhz bu səbəbə görə bəsit maddələr elementlərdən sayca çoxdur. Bəsit maddələr isə öz növbəsində birləşərək kimyəvi birləşmələri yəni mürəkkəb maddələri əmələ gətirir.
Mürəkkəb maddələrin təsnifatı
[redaktə | mənbəni redaktə et]Mürəkkəb maddələr iki böyük qrupa bölünür. Üzvi və qeyri-üzvi maddələr. Qeyri-üzvi maddələr isə 8 qrupa bölünür:Oksidlər,əsaslar,turşular,duzlar, intermetallid birləşmələr,binar birləşmələr,mürəkkəb ionlar və sərbəst radikallar.Bunlardan oksidlər,əsaslar,turşular və duzlar qeyri üzvi birləşmələrin əsas sinifləri adlanır.Oksidlər,əsaslar,turşular və duzlar arasında , ümumiyyətlə, qeyri-üzvi birləşmələr arasında genetik əlaqə mövcuddur.Bu genetik əlaqə onların mənşəyinin bir daha bir olduğunu sübut edir.Üzvi maddələr isə 2 böyük qrupa bölünür:Tsiklik və atsiklik birləşmələr.
Komplekslər haqqında qısa məlumat
[redaktə | mənbəni redaktə et]Kimyəvi birləşmələr isə daha da mürəkkəb maddələri kompleksləri yaradır.Kompleks birləşmələr isə adi mürəkkəb maddələrdən fərqlənir.Onlar iki sferadan : daxili və xarici sferadan ibarətdir.Burada mərkəzi və liqandlar olur. Mərkəzi ətrafında müəyyən sayda(əsasən:2,4,6,8) liqand olur.Liqandların sayı mərkəzi elementin koordinasiya ədədi adlanır.
Maddələrin adlandırılması
[redaktə | mənbəni redaktə et]Hər bir kimyəvi maddə özünəməxsus adla deyil ,daxil olduğu sinfin adlandırma qanunlarına görə adlandırılır.Oksidlərin adıandırılması sadədir.Elementin və oksigenin yunanca sayı deyilir.Məsələn , dinatrium -monooksid. Əsaslar da belə qayda ilə adlandırılır.Sadəcə burada oksigenin yox "OH" qrupunun sayı göstərilir.Məsələn, natrium-hidroksid.Turşuları adlandlrarkən əvvəlcə hidrogenin sonra oksigenin yunanca sayı daha sonra isə mərkəzi elementin adı və əsas valentliyi deyilir.Məsələn, hidrogen tetraokso sulfat (VI).Duzları adlandırarkən isə hidrogen əvəzinə metalın adı deyilir.Məsələn, natrium tetraokso sulfat (VI).
Kimyanın bölmələri
[redaktə | mənbəni redaktə et]Kimya üç böyük bölməyə ayrılır:[6]
Ancaq kimyanın başqa bölmələri də mövcuddur:
- Analitik kimya
- Nüvə kimyası
- Radiokimya
- Radioaktivlik kimyası
- Kvant kimyası
- Elektrokimya
- Kolloid kimyası
- Təbabət kimyası
- Metalüzvi kimya
- Enzimologiya (fermentlər kimyası)
- Fiziki kimya (fizikokimya)
- Kimyəvi termodinamika
- Termokimya və s.
Digər elmlərlə əlaqəsi
[redaktə | mənbəni redaktə et]Kimya daha çox fizika, biologiya və geologiya elmləri olmaqla digər təbiət elmləri ilə sıx əlaqədədir. Bu əlaqələr nəticəsində fiziki kimya, geokimya, biokimya və s. törəmə elm sahələri meydana çıxmışdır.[6]
Kimyanın digər elmlərlə əlaqəsi əsasən metodların ehtiyacı nəticəsində əmələ gəlir. Məsələn, biokimya elmi biologiyada canlı orqanizmlərin tərkibində olan maddələrin öyrənilməsində kimyəvi metodlara olan ehtiyac nəticəsində əmələ gəlmişdir. Həmçinin, fiziki kimya da əsasən analitik kimya elminin fiziki metodlara olan ehtiyacı nəticəsində əmələ gəlir. Geokimya elmi isə dövranları, süxurların, torpağın kimyəvi tərkibini öyrənir. Başqa sözlə, geokimya elmi geologiya elmində kimyaya olan ehtiyac nəticəsində yaranmışdır.
Üzvi maddələrin təsnifatı və adlandırılması
[redaktə | mənbəni redaktə et]Kimyaçılara məlum olan birləşmələrin sayının artım sürətini təssəvvür etmək belə,çox çətindir.Son 120 ildə üzvi maddələrin siyahısı 1500 dəfə artmışdır.[7] Bu maddələri nəhəng qoşun birləşməsinə bənzətmək olar.Belə sayda olan maddələri isə trivial adla adlandırmaq isə absurd olardı.Ona görə də hamı tərəfindən qəbul edilmiş ciddi adlandırma üsulu yaratmaq lazım idi.Alimlər tərəfindən, belə təsnifata ilk dəfə edilən cəhd üzvi kimyanın bir sərbəst elm kimi formalaşdığı bir dövrdə həyata keçirildi.1839-cu ildə fransız kimyaçısı Jan Batsit Düma(1800–1884) tiplər nəzəriyyəsini təklif etdi.[7] Alim eyni əsas reaksiyalarla xarakterizə olunan və oxşar quruluşlu maddələri bir tipə aid edirdi: spirt,turşu,aldehid,asetat,efir və s.Dümanın ideyaları onun həmyerlisi Şarl Frederik Jerarın işlərində inkişaf etdirilmişdir."Üzvi turşuların anhidridləri haqqında" məqaləsində Jerar təklif etdi ki, bütün üzvi maddələri dörd əsas qrupa bölmək olar:hidrogen,hidrogen xlorid,su və ammonyak.[7] Bu dörd tipə daxil olan maddələrdə hidrogen atomunu müəyyən atomlar qrupu ilə əvəz etməklə istəlinən üzvi maddəni almaq olar.O dövrdə kimyaçılar əvəzedici qrupların və bütövlükdə molekulun quruluşu haqqında heç nə bilmirdilər. Jerar hidrogen tipinə karbihidrogenləri,hidrogen-xlorid tipinə isə karbohidrigenlərin halogenli törəmələrini və nitrilləri aid edirdi. Su tipinə o,ən geniş öyrənilmiş və ən çoxsaylı turşuları, sadə və mürəkkəb efirləri, yurşu anihidridlərini və aldehidlərini daxil edirdi. Jerara görə ammonyak tipinə aminlər,amidlər,imidlər və s.aid olmalıdır.[8] Bu sistemdə rasional başlanğıcın olmasını qəbul etməmək olmaz.1842-ci ildə Yakob Şil belə bir ideya söylədi ki, spirtlər müəyyən sıra əmələ gətirir və bu sırada hər bir birləşmə özündən əvvəlki birləşmədən müəyyən atomlar qrupu ilə fərqlənir.Sonlar Jan Düma doymuş turşular üçün bu sıranı müəyyən etdi.Lakin o dövrdə üzvi birləşmələrin quruluşu haqqında məlumat az idi.Hətta məlum üzvi birləşmələrin dəqiq molekulyar formulu belə, məlum deyildi. XIX əsrin ikinci yarısında üzvi kimya yalnız eksperimental deyil, həm də nəzəri elm kimi güclü formalaşmağa başladı.Kimyaçılara məlum olan birləşmələrin sayı kəskin artı və tiplər nəzəriyyəsinə sığışmadı.1861-ci ildə Aleksandr Mixayiloviç Butlerov elmə, molekulda atomların birləşmə ardıcıllığını daxil etdi.[9][10][11][12] O quruluş nəzəriyyəsini yaratdı.Butlerov nəzəriyyəsi müasir təsnifatın başlanğıcı oldu.

Karbon skeletinin quruluşu,bu təsnifatın əsasını təşkil edirdi.Birləşmə,onun karbon zəncirinin quruluşundan asılı olaraq, müəyyən sinfə daxil edilirdi:şaxələnmiş və ya xətti;digər atomları saxlayan və ya yalnız karbon elementindən təşkil olunan;tsiklik qapalı və ya xətti uzanmış. Alman kimyaçıları Fridrix Avqust Kekule və Adolf Bayerin (1835–1917) aromatik birləşmələrin quruluşu sahəsində işlərindən sonra, yəni XIX əsrin ikinci yarısında, üzvi birləşmələrin "nəsil ağacına" oxşar təsnifat sxemi yaradıldı.[7] Üzvi birləşmələrinin təsnifatının digər prinsipi homoloji sıra və qruplar prinsipinə əsaslanır. Xassələrinə görə oxşar, tərkibinə görə isə bir-birindən CH2 qrupu-homoloji fərq qədər fərqlənən üzvi birləşmələrdə mövcuddur.Oxşar birləşmələrin sırası homoloji, üzvləri isə homoloqlar adlanır.Məsələn etilen, propen, buten və digər karbohidrogenlərCnH2n ümumi formuluna malik homoloji sıralar əmələ gətirirlər. Əksər homoloji sıraların üzvləri xarakterik funksional qrupa malik olurlar. Funksional qrup homoloqların ümumi kimyəvi xassələrini müəyyən edən atom və ya atomlar qrupu ola bilər.
Kimyəvi rabitə
[redaktə | mənbəni redaktə et]Atomların molekul və kristal qəfəs əmələ gətirməsində iştirak edən bütün qüvvələrin məcmusuna kimyəvi rabitə deyilir. Kimyəvi rabitələrin aşağı növləri ayırd edilir:
- Kovalent rabitə — ortaqlaşmış elektron cütü hesabına yaranan rabitə.[13]
- İon rabitə — kation və anionlar arasında yaranan rabitə.[14]
- Metallik rabitə — metallar arasında olan rabitə.[15]
- Hidrogen rabitəsi — molekullar arasında olan rabitə.[15]
Kovalent rabitə
[redaktə | mənbəni redaktə et]Kovalent rabitənin iki növü var:[13]
- Şərikləşmə yolu ilə yaranan rabitə;
- Donor- akseptor rabitəsi (Donor akseptor rabitəsi iki eyni atom arasında yarandıqda dativ rabitə adlanır).
Kovalent rabitənin növləri
[redaktə | mənbəni redaktə et]Orbitalların vəziyyətinə görə:[13]
- π rabitə
- σ rabitə
elektron sıxlığına görə:[13]
- polyar kovalent rabitə
- qeyri- polyar kovalent rabitə
İon rabitəsi
[redaktə | mənbəni redaktə et]İon rabitəli birləşmələr bunlardır:[14]
- metal halogenidlər
- əsaslar
- duzlar
Metallik rabitə
[redaktə | mənbəni redaktə et]Matal ionları arasında sərbəst elektronlar arasında yaranan rabitə metal rabitəsi və ya metallik rabitə adlanır.[15]
Hidrogen rabitəsi
[redaktə | mənbəni redaktə et]Hidrogen rabitəsi molekullararası rabitədir.[15]
Valent Rabitələr Nəzəriyyəsi (VRN)
[redaktə | mənbəni redaktə et]Valent rabitələr nəzəriyyəsində göstərilir ki, hər bir birləşmədə valintliyə sahibdir və bu onun əmələ gətirdiyi kovalent rabitələrin sayına bərabərdir.[7]
Molekulyar Orbitallar Nəzəriyyəsi (MON)
[redaktə | mənbəni redaktə et]MON- da göstərilir ki, molekullar çoxnüvəli hissəciklərdir və onların ətrafənda elektron örtüyü var.[7]
Kristal Sahə Nəzəriyyəsi (KSN)
[redaktə | mənbəni redaktə et]KSN- də göstərilir ki, bütün birləşmələrdə bir mərkəzi atom və onun ətrafında olan liqandlar mövcuddur.[7]
Katalizatorlar
[redaktə | mənbəni redaktə et]Katalizatorlar kimyəvi reaksiya sürətləndirir və bəzən onun gedişinə təsir edir. Amma reaksiyada nə reagent, nə də məhsul deyil.[7] Katalizatorların ən ixtisaslaşmış nümayəndələri enzimlər və ya fermentlərdir. Onları enzimologiya öyrənir.[16]
Fermentlər
[redaktə | mənbəni redaktə et]Fermentlər çoxludur: Katalaza, ribonukleaza, katalaza və s. Məsələn katalaza haqqında danışdıqda deyə bilərik ki, Katalaza hidrogen- peroksidi (H2O2) dihidrogen (H2) və dihidrogen- monooksidə (H2O, su) parçalayan enzimdir; (ferment)[17]. Tərkibində Fe3+ kationu saxlayır; bu günə qədər hidrogen peroksidi katalaza enzimindən sürətli parçalayan katalizator nə tapılmış, nə də sintez edilməmişdir; hidrogen peroksidlə əmələ gətirdiyi aralıq kompleks katalaza peroksidat (CAT-H2O2) adlanır; tənəffüs zamanı ağ ciyərlərimizdə hidrogen- peroksid alınır, bu maddə tibdə istifadə edilməsinə baxmayaraq zəhərlidir, bu səbəbdən orqanizmdə katalaza enziminə ( fermentinə )ehtiyac olur; katalaza demək olar ki, bütün aerob orqanizmlərdə tapılmışdır; katalaza dörd subvahiddən əmələ gəlmişdir və tərkibində təxminən 2 milyon aminturşu qalığı mövcuddur, yəni tetramerdir[18] ; bu dörd subvahiddə hidrogen- peroksidlə reaksiyaya daxil olmağa imkan verən hem var; İnsan orqanizmində katalaza üçün optimal pH=7-dir[19] pH- ın 6.8 və 7.5 kimi qiymətlərində reaksiya getmir;[20] Digər orqanizmlər üçün bu qiymət 6–11 arası qiymətlər alır[21] ; optimal temperatur isə müxtəlif orqanizmlər üçün müxtəlifdir;[22] . İnsan katalazasını konseptual dörd bölməyə bölmək olar ki, bu dörd bölmə birlikdə tetramer təşkil edir[23].Hər qlobulada geniş hidrofob əsaslı 8 antiparalel b-barel vardır (b1–8) və bir tərəfdən A9 loops ilə əhatə olunmuşdur[23].b-barel üzərindəki A Helikal domayn b4 və b5 qalıqları arasında əldə olunan dörd C-terminal Helikes (A16, A17, A18 və A19) və dörd Helikesdən ibarətdir (A4, A5, A6, və a7)[23]. 1818-ci ildə Louis Jacques Thenard səhvən hidrogen peroksidi parçalayan enzim tapır. Bu enzim katalaza idi. Bu enzim sonradan bir çox orqanizmlərdə tapıldı və Oscar Loew 1900-cü ildə bu enzimi katalaza adlandırmağı təklif etdi[24]
İstinadlar
[redaktə | mənbəni redaktə et]- ↑ Uqay Y.A. Ümumi kimya. Bakı: "Çaşıoğlu" nəşriyyatı. 2004. səh. səh 5. (#accessdate_missing_url)
- ↑ İ.Lətifov,A.Orucova,X.Zeynalova. Kaspi.Orta məktəb şagirdləri və abituriyentlər üçün vəsait..Kimya. Bakı: "Polygraphing Production" nəşriyyatı. 2012. səh. səh 5. (#accessdate_missing_url)
- ↑ Məmmədov, Elman; Abışov, Nasim; Süleymanov, Rahim. Uşaqlar üçün Kimya ensiklopediyası. Şərq-Qərb. 8. ISBN 978-9952-34-195-9. (#accessdate_missing_url)
- ↑ V.S. Həsənov, Y.C. Qasımova , G.V. Babayeva, A.M. Umudova. Kimya həvəskarları üçün yaddaş. Bakı: Elm. 2013. ISBN 978-9952-453-03-4-655. (#accessdate_missing_url)
- ↑ "Arxivlənmiş surət". 2016-10-12 tarixində orijinalından arxivləşdirilib. İstifadə tarixi: 2014-09-19.
- ↑ 1 2 Abbasov M., Abbasov V., Abışov N., Əliyev V. Kimya (Ümumtəhsil məktəblərinin 7-ci sinfi üçün dərslik). Bakı: Aspoliqraf. 2014. (#accessdate_missing_url)
- ↑ 1 2 3 4 5 6 7 8 E.Məmmədov,N.Abışov,R.Süleymanov,E.Allahyarov. Uşaqlar üçün Ensiklopediya.Kimya. Bakı: "Şərq-Qərb" nəşriyyatı. 2008.
- ↑ E.Məmmədov,N.Abışov,R.Süleymanov,E.Allahyarov. Uşaqlar üçün Ensiklopediya.Kimya. Bakı: "Şərq-Qərb" nəşriyyatı. 2008. səh. səh 334. (#accessdate_missing_url)
- ↑ İ.Lətifov,A.Orucova,X.Zeynalova. Kaspi.Orta məktəb şagirdləri və abituriyentlər üçün vəsait..Kimya. Bakı: "Polygraphing Production" nəşriyyatı. 2012. səh. səh 157. (#accessdate_missing_url)
- ↑ V.Abbasov,A.Məhərrəmov,M.Abbasov,V.Əliyev,R.Əliyev,A.Əliyev,L.Qasımov. Dərslik .10-cu siniflər üçün .Kimya. Bakı: "Aspoliqraf" nəşriyyatı. 2005. səh. səh 39. (#accessdate_missing_url)
- ↑ İ.Lətifov,Ş.Mustafa. Dərslik.9-cu siniflər üçün.Kimya. Bakı: "Şərq-Qərb" nəşriyyatı. 2016. səh. səh 147. (#accessdate_missing_url)
- ↑ M.Abassov. TQDK.Qəbul imtahanlarına hazırlaşanlar,yuxarı sinif şagirdləri və müəllimlər üçün dərs vəsaiti.Kimya. Bakı: "Şərq-Qərb" nəşriyyatı. 2008. səh. səh 134. (#accessdate_missing_url)
- ↑ 1 2 3 4 İ.Lətifov,A.Orucova,X.Zeynalova. Kaspi.Orta məktəb şagirdləri və abituriyentlər üçün vəsait..Kimya. Bakı: "Polygraphing Production" nəşriyyatı. 2012. səh. səh 38. (#accessdate_missing_url)
- ↑ 1 2 İ.Lətifov,A.Orucova,X.Zeynalova. Kaspi.Orta məktəb şagirdləri və abituriyentlər üçün vəsait..Kimya. Bakı: "Polygraphing Production" nəşriyyatı. 2012. səh. səh 41. (#accessdate_missing_url)
- ↑ 1 2 3 4 İ.Lətifov,A.Orucova,X.Zeynalova. Kaspi.Orta məktəb şagirdləri və abituriyentlər üçün vəsait..Kimya. Bakı: "Polygraphing Production" nəşriyyatı. 2012. səh. səh 42. (#accessdate_missing_url)
- ↑ fermentlər
- ↑ Chelikani P, Fita I, Loewen PC. "Diversity of structures and properties among catalases". Cellular and Molecular Life Sciences. 61 (2). January 2004: 192–208. doi:10.1007/s00018-003-3206-5. ISSN 1420-682X. PMID 14745498.
- ↑ Boon EM, Downs A, Marcey D. "Catalase: H2O2: H2O2 Oxidoreductase". Catalase Structural Tutorial Text. 2019-10-22 tarixində arxivləşdirilib. İstifadə tarixi: 2007-02-11.
- ↑ Maehly AC, Chance B. "The assay of catalases and peroxidases". Methods of Biochemical Analysis. Methods of Biochemical Analysis. 1. 1954: 357–424. doi:10.1002/9780470110171.ch14. ISBN 978-0-470-11017-1. PMID 13193536.
- ↑ Aebi H. "Catalase in vitro". Methods in Enzymology. Methods in Enzymology. 105. 1984: 121–6. doi:10.1016/S0076-6879(84)05016-3. ISBN 978-0-12-182005-3. PMID 6727660.
- ↑ "EC 1.11.1.6 – catalase". BRENDA: The Comprehensive Enzyme Information System. Department of Bioinformatics and Biochemistry, Technische Universität Braunschweig. 2013-11-03 tarixində arxivləşdirilib. İstifadə tarixi: 2009-05-26.
- ↑ Toner K, Sojka G, Ellis R. "A Quantitative Enzyme Study; CATALASE". bucknell.edu. 2000-06-12 tarixində arxivləşdirilib. İstifadə tarixi: 2007-02-11.
- ↑ 1 2 3 Putnam CD, Arvai AS, Bourne Y, Tainer JA. "Active and inhibited human catalase structures: ligand and NADPH binding and catalytic mechanism". Journal of Molecular Biology. 296 (1). February 2000: 295–309. doi:10.1006/jmbi.1999.3458. PMID 10656833.
- ↑ Loew O. "A New Enzyme of General Occurrence in Organisms". Science. 11 (279). May 1900: 701–2. Bibcode:1900Sci....11..701L. doi:10.1126/science.11.279.701. JSTOR 1625707. PMID 17751716.