Aromatik karbohidrogenlər
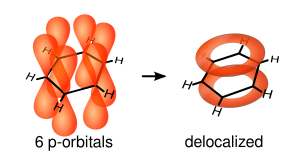
Aromatik karbohidrogenlər - molekullarında bir və ya bir neçə benzol həlqəsi olan karbohidrogenlərə aromatik karbohidrogenlər deyilir. Aromatik karbohidrogenlər[1] dedikdə benzol və xassəcə ona bənzər birləşmələr nəzərdə tutulur. Belə ki, aromatik karbohidrogenlər onları başqa birləşmələrdən fərqləndirən və adətən aromatik xassə adlanan bir sıra xüsusiyyətlərə malikdir.[2][3][4] Tərkibinə daxil olan benzol nüvəsinin sayından və onların arasındakı əlaqənin xarakterindən asılı olaraq aromatik karbohidrogenlər iki qrupa bölünür:
- Bir benzol nüvəli aromatik karbohidrogenlər. Bu qrupa benzol və onun homoloqları daxildir.
- Kondensləşmiş və ya kondensləşməmiş bir neçə benzol nüvəli aromatik karbohidrogenlər. Bu qrupa difenil, difenilalkanlar, naftalin, fenantren, antrasen, asenaften, flüoren və b. daxildir.
Aromatik karbohidrogenlərin beynəlxalq adı Arenlər-dir.[5] Aromatik karbohidrogenlərin ən sadə nümayəndəsi benzoldur. Benzol homoloqlarının düsturu CnH2n-6 kimidir. Aşağıdakı qalereyada Arenlərin bir sıra nümayəndələri göstərilmişdir:
- Arenlər
-
Toluol
-
Etilbenzol
-
Stirol
-
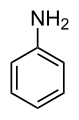
Anilin
Bir benzol nüvəli aromatik karbohidrogenlər[redaktə | mənbəni redaktə et]
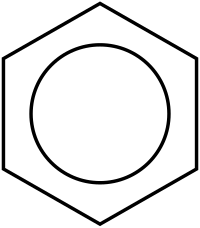
1865-ci ildə Alman alimi Fridrix Avqust Kekule (Bonn Universitetini bitirmişdir) Benzola tsikloheksatrien kimi quruluş vermişdir[6]. (C6H6). Sonralar benzol üçün daha bir sıra quruluşlar təklif olunmuşdur. Kekule formulundan bu günə kimi istifadə olunmasına baxmayaraq o benzolun xassələrini tam əks etdirmir.[7][8][9] Belə ki, Kekule formulu benzolun birləşmə reaksiyasına daxil olmasını izah etdiyi halda, benzol üçün birləşmə reaksiyasının deyil, əvəzlənmə reaksiyasının xarakter olması, onun termodinamik və oksidləşdiricilərə qarşı davamlığı izah olunmamış qahrdı. Digər tərəfdən Kekule formuluna görə benzolun izomerdən 1,2-diəvəzli törəmələri ikidən ibarət olmalıdır. Lakin belə izomerlərin olması heç vaxt müşahidə olunmamışdır. Kekule bunu düzgün olaraq benzolda ikiqat əlaqələrin osillasiyası (yerlərini dəyişməsi) ilə izah edirdi.
Çox da uzaq olmayan (1960-1970-ci illər) illərdə müəyyən edilmişdir ki, benzol 253.7nm dalğa uzunluqlu şüa ilə işıqlandırıldıqda, o, Klaus, Düar və Xükkel quruluşlanna keçir. Həmin quruluşlarda C6H6-nm xassələri Kekule quruluşlu C6H6-dan kəskin fərqlənir: onlar asan (o cümlədən KMn04-lə) oksidləşir və sürətlə bromlaşır. Əldə edilən məlumatlar benzolun Kekule quruluşunda mövcud olması fikri ilə yaxşı izah olunur.
Hazırda müxtəlif üsullarla təsdiq edilmişdir ki, benzol molekulu koplanardır, yəni benzolda bütün atomlar bir müstəvi üzərində yerləşir və karbon atomlarındakı qoşulmuş π - elektron orbitalları həmin müstəviyə perpendikulyardır.
Kekule formulunda benzol ehtimal olunduğundan termodinamik daha sabitdir. Belə ki, tsikloheksenin tsikloheksana hidrogenləşmə enerjisi 119,7 kC/Mol təşkil etdiyi halda, üç ikiqat rabitəli benzol tsikloheksana hidrogenləşdikdə ehtimal olunan qədər, yəni 119,7x3=359,1 kC/Mol deyil, ondan 150,7 kC/Mol az enerji ayrılır. Benzolun təcrübi tapılmış yanma istiliyi də nəzəri hesablanmışdan bir o qədər azdır. Həmin enerjiyə (150,7 kC/Mol) benzolun sabitləşmə və ya rezonans enerjisi deyilir. 1945-ci ilə kimi benzol üçün Kekule formulundan istifadə olunmuşdur. Rezonans nəzəriyyəsi meydana çıxdıqdan sonra isə benzola iki Kekule quruluşunun rezonans hibridi kimi baxılmışdır. Bu o deməkdir ki, benzol ayrıldıqda götürülən həmin quruluşların heç birində deyil, ancaq onların rezonans hibridi formasında mövcud olur.[10][11].
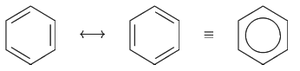
Quruluş[redaktə | mənbəni redaktə et]
1865-ci ildə Kekule benzola tsikloheksatrien kimi quruluş vermişdir. Sonralar benzol üçün daha bir sıra quruluşlar təklif olunmuşdur. Bu quruluşlar aşağıdakı qalereyada daha ətraflı göstərilmişdir:
-
Klaus formulu
-
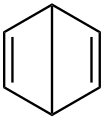
Düarın xinoid formulu
-
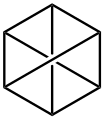
Laderburq formulu
-
Bayerin mərkəzli formulu
-
Tile formulu
-
Kekule formulu
-
Benzolun günbəz modeli
Adlandırılması[redaktə | mənbəni redaktə et]
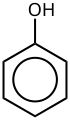
Arenlərin bərk nümayəndələri benzol sözü əlavə etməklə oxunur.Məs. Xlorbenzol, Brombenzol, Etilbenzol, Nitrobenzol və s. Bəzi törəmələrin əvəzləyicinin adı ilə əlaqəsi olmayan xüsusi adlan vardır.Məs. Toluol, Anilin, Fenol, Bluzosulfoturşu və s. Əgər benzol halqasında bir neçə əvəzləyici olarsa, belə törəmələri adlandırmaq üçün əvəzləyicilərin adlarından başqa, onların yerləşmələrini də göstərmək lazımdır.Məs. Orto dixlor benzol, Meta dixlor benzol, Para dixlor benzol və s.
İki əvəzləyici xüsusiyyətlərinə görə fərqli olduqda və onların adlarının "benzol" sözü ilə birləşməsi xüsusi ada uyğun gəlmədikdə, belə birləşmənin adında əvəzləyicilərin adları "benzol" sözündən əvvəl yazılır, məsələn, xlorbrombenzol, bromnitrobenzol və s. Əgər əvəzləyicinin birinin adı "benzol" sözü ilə xüsusi adların birinə uyğundursa, onda birləşmə həmin xüsusi adlı birləşmənin törəməsi kimi adlanır.Məs. Orto- nitrotoluol, Para - bromfenol, Meta - nitrobenzoy turşusu, Para - yodanilin və s. Benzol halqasında ikidən çox əvəzləyici olduqda onların molekuldakı vəziyyəti rəqəmlərlə göstərilir.Məs. 1,2,4 –tribrombenzol, 2 xlor 4 nitro fenol, 2 dinitrotoluol, 2,6 dibrompropan və s.
Təsnifat[redaktə | mənbəni redaktə et]

Aromatik karbohidrogenlərin təsnifatını aşağıdakı kimi vermək olar:
6 p-elektronlar Sistemi
- Benzol və onun homoloqları.
- Tsiklopentadienil-anionu.
- Tsikloheptatrienil-kationu.
- Tsiklobutadienin anionu.
- Pirrol, Furan, Tiofen, Pirridin.
10 p-elektronlar Sistemi
- Naftalin.
- Naftalinin izomeri Anulen.
- Tsiklooktatetraen Dianionu.
- İndol, Xinolin, İzoxinolin, Xinazolin, Xinooksalin, və başqa sistemlər, Benzol üzüyü əsasında formalaşanlar.
- Xinolizidin, Pirrolizidin, Purin, Pteridin (və onların homoloqları).
14 p-elektronlar Sistemi
- Antratsen, Fenantren, Fenalen.
- 14-Annulen.
14 p-elektronlardan çox Sistemlər
Homoaromatik birləşmələr
- Eynicinsli birləşmələrdir. Xarici orbitalında sp³ hibridləşməsi saxlanılır.
Sidnonlar
- Mezoion birləşmələr.
Spiroaromatik sistemlər
- 4,2-Spiraren. Hükkel qaydasına tabe olur.
Aromatik karbohidrogenlərin struktur formulları[redaktə | mənbəni redaktə et]
Arenlər müxtəlif struktur formullara malikdirlər. Onlardan bəzilərini nəzərdən keçirək. Aromatik karbohidrogenlərin ən sadə nümayəndəsi benzoldur. Benzolun struktur formulu aşağıdakı kimidir:

Kekule benzolun formulunu aşağıdakı kimi göstərmişdir:

Naftalinin struktur formulu aşağıdakı kimidir:

Toluolun struktur formulu aşağıdakı kimidir:

Tsimolun struktur formulu aşağıdakı kimidir:

Dimetilbenzollar[redaktə | mənbəni redaktə et]
Dimetilbenzollar aşağıdakılardır:
-
o-ksylen
(1,2-dimetilbenzol) -
m-ksylen
(1,3-dimetilbenzol) -
p-ksylen
(1,4-dimetilbenzol)
Alınma üsulları[redaktə | mənbəni redaktə et]
Arenlərin alınma üsulları aşağıdakı üsullardan asılıdır:
- Daş kömürün quru distilləsindən. Bu proses 10000 – 13000 S –də koks peçlərində aparılır. Bu zaman aşağıdakı fraksiyalar alınır:
- Koks
- Daş kömür qətranı
- Ammoniyaklı su
- Koks qazı
- Daş kömür qətranı fraksiyasından aromatik birləşmələr və fenol alınır → benzol, toluol, naftalin, fenol və s. alınır;
- Neftdən alırlar (ural neftində 60% aromatik k/h-lər var). Neft məhsullarını 7000 S temperaturda → 15-18% aromatik k/h-lər alınır;
- Heksandan alınır;
- Tsikloheksandan katalizator iştirakı ilə qızdırmaqla;
- N. Zelinski və V. Kazanski üsulu ilə;
- Benzol və onun homoloqları Fridel - Krafts üsulu ilə alkilhallogenlərə AlCl3, SnCl4, BF3 benzol q/t alınır. reaksiyanı həm sənayedə həm də laboratoriyada həyata keçirmək olar.
- Benzolun hallogenli törəmələrindən Vürs-Fittiq reaksiyası vasitəsilə alkilbenzollar alınır.
Aromatik karbohidrogenlərin sənaye mənbələri[redaktə | mənbəni redaktə et]
1. Aromatik karbohidrogenlərin əsas mənbəyi daş kömür qətranıdır. Aromatik birləşmələrin kömürün kokslşmasından alınmasına baxmayaraq onların əsas mənbəyi neftdir.
2. Bəzi neftləri (Orta Asiya) birbaşa distillə etməklə aromatik karbohidrogenləri almaq olur. Ancaq, əksər kütlə aromatik birləşmələri yüksək temperatur və katalizatorun iştirakı ilə neft fraksiyalarının aromatikləşməsindən alırlar. Katalizatorların (alüminium molibdat və ya alüminium oksid üzərində platin), yüksək temperaturun (500...700oC) və təzyiqin (10..40atm) təsiri ilə aparılan proses katalitik riforminq adlanır. Bu cür proseslərin nəticəsində alkanların tsiklodehidrogenləşdirilməsi , tsikloalkanların dehidrogenləşməsi və izomerləşməsi reaksiyalaraı gedir. Burada həmçinin toluolda alınır. Benzola olan tələbatı tam ödəmək üçün böyük həcmdə toluolu dealkilləşdirib benzola çevirirlər. Reaksiyanı xrom oksidi, sealitlərin iştirakı ilə və ya termiki yolla aparırlar.
Katalitik reaksiya[redaktə | mənbəni redaktə et]
Aromatik karbohidrogenlərin katalitik reaksiyası:
Vürs-Fittiq reaksiyası[redaktə | mənbəni redaktə et]
Vürs-Fittiq reaksiyası vasitəsilə alkilbenzollar alınır:
Fridel-Krafts reaksiyası[redaktə | mənbəni redaktə et]
Benzol və onun homoloqları Fridel - Krafts üsulu ilə alkilhallogenlərə AlCl3, SnCl4, BF3 (Lyuis turşuları)benzol q/t alınır:
Fiziki xassələri[redaktə | mənbəni redaktə et]
Arenlər suda həll olmurlar. Üzvi həlledicilərdə həll olurlar, izomerlərin sayı sıx olarsa qaynama temperaturu çox olur. Arenlər özləri yaxşı həlledicidirlər. Hisli alovlu yanırlar ( C-çox olduğuna görə). Ərimə və qaynama temperaturu müvafiq C olan alkan, alken və alkinlərdən çoxdur.
Aromatik ionlar[redaktə | mənbəni redaktə et]

Təbiətdə aromatik ionlar mövcuddur. Hüggel qanununa görə, əgər 2π elektronu sistemə qoşulursa, onda bu aromatik ion hesab olunur:

Tsiklopentadienin strukturu:
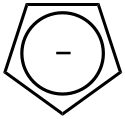
Kimyəvi reaksiyalar[redaktə | mənbəni redaktə et]
Aromatik karbohidrogenlər müxtəlif orqanik karbohidrogenlərlə reaksiyaya girir.
Aromatik əvəzləmə[redaktə | mənbəni redaktə et]
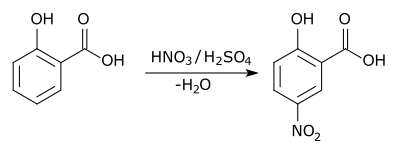
Sulfat turşusunun nitratlaşması[14]:
Reaksiyalar arasında əlaqə[redaktə | mənbəni redaktə et]
Aromatik karbohidrogenlərin reaksiyaları arasında aşağıdakı əlaqə mövcuddur[15]:
Hidratlaşma[redaktə | mənbəni redaktə et]
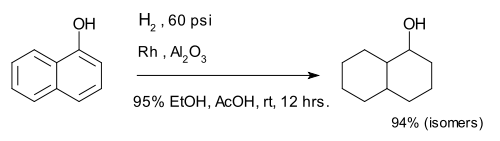
Aromatik karbohidrogenlərin hidratlaşması reaksiyası üzüyə bənzər forma yaradır[16]:
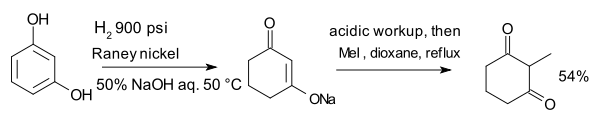
Rezorsin olan mürəkkəb maddə, sulu natrium hidroksidin iştirakı Reney nikel ilə hidrogenləşdirilmiş 2-metil-1,3-sikloheksandion üçün metil yodlu ilə alkili edən Enoliti təşkil edir[17]:
Ozonlaşma[redaktə | mənbəni redaktə et]
Benzolun ozonla qarşılıqlı təsirindən ozonidlər alınır və nəmin təsirindən parçalanaraq, üç molekul dialdehid əmələ gətirir. Ancaq, benzol üçün əsasən üç tip elektrofil, nukleofil və sərbəst radikal əvəzolunma reaksiyaları xarakterikdir.
Elektrofil əvəzolunma reaksiyaları (SE)[redaktə | mənbəni redaktə et]
Bu benzol nüvəsi üçün tipik reaksiyadır. Qeyd etdiyimiz kimi benzol həlqəsinin yerləşdiyi müstəvinin yuxarı və aşağısında altı π-elektronlarından ibarət delokalizə olunmuş sistem vardır. Bu faktiki olaraq lokalizə olunmuş doymamış rabitələrdən möhkəmdir. Onun qırılması üşün daha çox enerji tələb olunur. Bu cür π-elektronlar elektron çatışmazlığı hiss edən hissəciklərin (elektrofil) hücumu üçün daha əlverişlidir. İkiqat rabitənin π-elektronları adətən molekulun iki zərrəciyini özünə birləşdirməyə can atdığı halda, benzolun delokalizə olunmuş π-elektronları daha davamlı olduğundan bu sistemi qırmağa meyilli deyillər. Buna gğrə benzol üçün əsasən elektrofil əvəzolunma reaksiyası xarakterikdir.
Aromatik nüvədə nukleofil əvəzetmə[redaktə | mənbəni redaktə et]
Aromatik birləşmələr üçün nukleofil əvəzetmə elektrofil əvəzetməyə nisbətən az xarakterikdir. Əvəz olunmamış benzol bu tip reaksiyalara ümumiyyətlə daxil olmur. benzol nüvəsində elektron sıxlığını azaldan elektroakseptor qruplar nukleofil əvəzetmə üçün imkan yaradır. Məsələn, xlorbenzolu fenola çevirmək üçün 300oC və 50 atm. təzyiq tələb olunduğu halda nitroxlorbenzol bu cür reaksiyalara aşağı temperaturda daxil olur. Reaksiyanın mexanizmi iki mərhələdən ibarətdir. Birinci mərhələdə nukleofil ikinci növ əvəzləyicisi ()X_ olan benzol nüvəsinə hüçüm edərək, onunla σ-rabitəsini əmələ gətirir və beş karbon atomları üzərində mənfi yükü olan qeyri-stabil delokalizə olunmuş zərrəciyə çevrilir. Nəticədə karbanion σ-kompleksini əmələ gətirir. İkinci mərhələdə X- anionu qopararaq aromatik həlqə bərpa olunur.
Aromatik nüvədə sərbəst radikal əvəzlənməsi[redaktə | mənbəni redaktə et]
- A-B+R' → A-R + B′ (SR)
Aromatik birləşmələrdə sərbəst radikal və ya homolotik əvəzetmə çox az rast gəlinir. Ən çox hidrogen atomu əvəz olunur. Əvəz edən adətən alkin və aril radikalları olur. Radikal əvəzolunmanın analoji olaraq ion əvəzlənməsi belədir: Birinci mərhələdə davamsız tsiklik radikal və ya cütləşməmiş elektronu olan radikallı σ-əmələ gəlir. Əgər reaksiyaya əvəzlənmiş benzol daxil olarsa, onda əsasən para və orto-izomerlər əmələ gəlir. Məsələn, metil yodidin benzolda fotolizi nəticəsində metil radikalı əmələ gəlir və reaksiya nəticəsində toluol və hidrogen yodid alınır:
- CH3J→hνCH3′ + J′
Aromatikləşmə[redaktə | mənbəni redaktə et]
Aromatik karbohidrogenlərin aromatik pilləsi üzük seqmenti üçün müxtəlif ola bilər[18]:
- Aromatikləşmə
-
Fenatren
-
Antratsen
-
Xrizen
-
"Klar" qanunu
Aromatik birləşmələr[redaktə | mənbəni redaktə et]
Təbiətdə aşağıdakı cədvəldə verilmiş aromatik karbohidrogen birləşmələri mövcuddur:
| Kimyəvi birləşmə | Kimyəvi birləşmə | ||
|---|---|---|---|
| Antritsin | Benzpiren və ya Benz(a)piren | 
| |
| Xrizen | 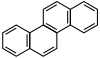 |
Koronin | 
|
| Koranilin | 
|
Tetrasin | |
| Naftalin | Pentasin | ||
| Finantrin | Pirin | 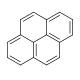
| |
| Trifenilin | 
|
Ovalin | 
|
Aromatik karbohidrogenlər[redaktə | mənbəni redaktə et]
- Arenlər
-
Toluol
-
O-Ksilol
-
P-Ksilol
-
M-Ksilol
-
Mseitilin və ya 1-3-5 Trimetilbenzol
-
1-2-4-5 Tetrametilbenzol
-
2-Finilheksan
-
Difenil və ya Bifenil
-
Anilin
-
Nitrobenzol
-
Benzoy turşusu
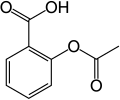
-
Paratsetamol
-
Trinitrofenol
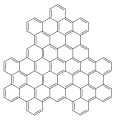
-
Superfenalin
-
Zetrin
-
Tetrafenil
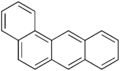
-
Benzantrisin
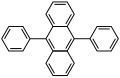
-
9,10-difenilantrisin
Aromatik karbohidrogenlərin Politsiklik quruluşu[redaktə | mənbəni redaktə et]
- Politsiklik quruluş
-
Politsiklik quruluşlu Aromatik karbohidrogenlər Kainatda
-
Politsiklik quruluşlu Aromatik karbohidrogenlər Təbiətdə
Ədəbiyyat[redaktə | mənbəni redaktə et]
- Грандберг И.И. Органическая химия. Москва, «Высшая школа», 1980.
- Баркан Я.Г. Органическая химия. Москва, «Высшая школа», 1980.
- Шаваров Ю.С. Органическая химия. Москва, Издательства химия, 2002.
- Петров А.А., Трафимов А.Т. Органическая химия. Санкт- Петербург, 2002.
- Qarayev Ş.F., İmaşev İ.B., Talıbov G.M.Üzvi kimya, Bakı, 2003.
- Məhərrəmov A.M., Məhərrəmov M.M. Üzvi kimya, BDU, Bakı, 2007.
- Məhərrəmov A.M.,Allahverdiyev M.Ə. Üzvi kimya, BDU, Bakı, 2007.
- Дж. Марч. Органическая Химия. Реакции, механизмы и структура. 1 том.
- Керри. Сандберг. Органическая химия. Механизмы реакций. 1 том.
- Химическая Энциклопедия в 5 томах. ред. И. Л. Кнунянц. 1 том.
- Українська радянська енциклопедія. У 12-ти томах. / За ред. М. Бажана. (Mikola Bajan) — 2-ге вид. — К., 1974—1985.
- Дж. Марч. Органическая Химия. Реакции, механизмы и структура. М.: «Мир», 1987.
- Керри Ф., Сандберг Р. Углубленный курс органической химии. М.: «Химия», 1981.
- Шабаров Ю.С. Органическая химия. М.: «Химия», 1994. Т.1,2.
- Зык Н.В., Белоглазкина Е.К. Ароматичность и ароматические углеводороды. М.: «КолосС»,2005
- Терней А. Современная органическая химия. М.: Мир, 1981. Т.1,2.
- И.И. Грандберг. Органическая химия. М.: «Высшая школа»,1980.
- Терней А. Л. Современная органическая химия. т.1. с. 578.
İstinadlar[redaktə | mənbəni redaktə et]
- ↑ Definition IUPAC Gold Book Link Arxivləşdirilib 2009-09-29 at the Wayback Machine
- ↑ P. v. R. Schleyer, "Aromaticity (Editorial)", Chemical Reviews, 2001, 101, 1115-1118. DOI: 10.1021/cr0103221 Abstract.
- ↑ A. T. Balaban, P. v. R. Schleyer and H. S. Rzepa, "Crocker, Not Armit and Robinson, Begat the Six Aromatic Electrons", Chemical Reviews, 2005, 105, 3436-3447. DOI: 10.1021/cr0103221 Abstract.
- ↑ P. v. R. Schleyer, "Introduction: Delocalization-π and σ (Editorial)", Chemical Reviews, 2005, 105, 3433-3435. DOI: 10.1021/cr030095y Abstract.
- ↑ Mechanisms of Activation of the Aryl Hydrocarbon Receptor Arxivləşdirilib 2012-02-17 at the Wayback Machine by Maria Backlund, Institute of Environmental Medicine, Karolinska Institutet
- ↑ Габриелян О.С., Остроумов И.Г. "Настольная книга учителя химии - 10 класс"
- ↑ P. v. R. Schleyer, "Aromaticity (Editorial)", Chemical Reviews, 2001, 101, 1115-1118. DOI: 10.1021/cr0103221 Abstract.
- ↑ A. T. Balaban, P. v. R. Schleyer and H. S. Rzepa, "Crocker, Not Armit and Robinson, Begat the Six Aromatic Electrons", Chemical Reviews, 2005, 105, 3436-3447. DOI: 10.1021/cr0103221 Abstract.
- ↑ P. v. R. Schleyer, "Introduction: Delocalization-π and σ (Editorial)", Chemical Reviews, 2005, 105, 3433-3435. DOI: 10.1021/cr030095y Abstract.
- ↑ A. W. Hofmann, "On Insolinic Acid," Proceedings of the Royal Society, 8 (1855), 1-3.
- ↑ The structure of cycloid hydrocarbons Henry Edward Armstrong Proceedings of the Chemical Society (London), 1890, 6, 95 - 106 Abstract
- ↑ Дж. Марч. Органическая Химия. Реакции, механизмы и структура. 1 том. с 88
- ↑ Терней А. Л. Современная органическая химия. т.1. с. 578.
- ↑ Webb, K.; Seneviratne, V. (1995). "A mild oxidation of aromatic amines". Tetrahedron Letters 36 (14): 2377–237810.doi:1016/0040-4039(95)00281-G
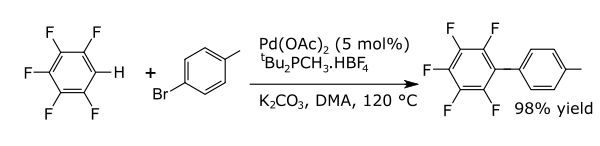
- ↑ afrance, M.; Rowley, C.; Woo, T.; Fagnou, K. (2006). "Catalytic intermolecular direct arylation of perfluorobenzenes.". Journal of the American Chemical Society 128 (27): 8754–8756. doi:10.1021/ja062509l
- ↑ Organic Syntheses, Coll. Vol. 6, p.371 (1988); Vol. 51, p.103 (1971). http://orgsynth.org/orgsyn/pdfs/CV6P0371.pdf Arxivləşdirilib 2012-04-16 at the Wayback Machine
- ↑ Organic Syntheses, Coll. Vol. 5, p.743 (1973); Vol. 41, p.56 (1961). http://orgsynth.org/orgsyn/pdfs/CV5P0567.pdf Arxivləşdirilib 2012-02-19 at the Wayback Machine
- ↑ title=Polycyclic Hydrocarbons 1964 LCCN 63012392}}
Xarici keçidlər[redaktə | mənbəni redaktə et]
- ATSDR - Toxicity of Polycyclic Aromatic Hydrocarbons (PAHs) (ing.)
- Fused Ring and Bridged Fused Ring Nomenclature (ing.)
- Database of PAH structures Arxivləşdirilib 2005-01-17 at the Wayback Machine (ing.)
- National Pollutant Inventory: Polycyclic Aromatic Hydrocarbon Fact Sheet Arxivləşdirilib 2006-05-18 at the Wayback Machine (ing.)
- Understanding Polycyclic Aromatic Hydrocarbons Arxivləşdirilib 2006-06-23 at the Wayback Machine (ing.)
- Astrobiology magazine Arxivləşdirilib 2007-09-29 at the Wayback Machine (ing.)
- Oregon State University Superfund Research Center (ing.)
- Carcinogenic FAC list Arxivləşdirilib 2007-11-28 at the Wayback Machine (ing.)
- Toxicological profiles of PAH (ing.)
- LIST of PAH Arxivləşdirilib 2008-10-11 at the Wayback Machine (ing.)
- Abiogenic Gas Debate 11:2002 (EXPLORER) (ing.)
- Hückel-Regel Arxivləşdirilib 2007-08-13 at the Wayback Machine
- Vorlesungsskript Arxivləşdirilib 2011-11-29 at the Wayback Machine
- aromáticos [ölü keçid]
- Estructuras interactivas de alguns hidrocarbonetos aromáticos
- Ю. В. Зефиров, П. М. Зоркий, Ван-дер-ваальсовы радиусы атомов в кристаллохимии и структурной химии (rus.)
- Н. Ф. Степанов, Химическая связь в простых двухатомных молекулах (rus.)
- Composti aromatici Arxivləşdirilib 2008-12-09 at the Wayback Machine
- Esperienze in laboratorio - Gli idrocarburi aromatici